فهرست عناوین
- مقدمه
- ویژگی های شیمیایی سوخت متانول
- ویژگی های اشتعال پذیری متانول
- ویژگی های احتراق و حدود اشتعال متانول
- ملاحظات ایمنی در برابر آتش سوزی متانول
- محتوای انرژی و ارزش حرارتی متانول
- ویژگی های احتراق و آلایندگی متانول
- متانول در برابر بنزین: بازده انرژی و عملکرد
- مقایسه ویژگی های متانول، اتانول، بنزین و گازوئیل
- متانول در موتورهای درون سوز
- پیل های سوختی مستقیم متانول و بازده آنها
- روش های تولید متانول و منابع انرژی
نوشته شده توسط شرکت صنایع متانول ایران
منتشر شده توسط شرکت صنایع متانول ایران
تاریخ انتشار مقاله : 07-09-1404
تاریخ بروزرسانی مقاله : 07-09-1404
تعداد کلمات : 3200
آدرس مقاله : لینک مقاله
قابلیت اشتعال و انرژی زایی متانول

مقدمه
متانول که به نام الکل متیلیک نیز شناخته می شود، یک ترکیب شیمیایی ساده است که به عنوان یک سوخت جایگزین توجه زیادی را به خود جلب کرده است. این ماده مایعی بی رنگ و فرار است، به شدت قابل اشتعال بوده و در هنگام سوختن انرژی آزاد می کند؛ ویژگی هایی که آن را در کاربردهای مختلف انرژی مفید می سازد. این مقاله مروری جامع بر ویژگی های اشتعال پذیری و بازده انرژی متانول ارائه می دهد و بررسی می کند که چگونه خصوصیات شیمیایی آن بر رفتارش به عنوان سوخت تأثیر می گذارد. در ادامه خطرات آتش سوزی متانول، خواص اشتعال آن و مقایسه محتوای انرژی آن با سوخت های رایج مانند بنزین و گازوئیل بررسی خواهد شد. علاوه بر این، به کاربرد متانول در موتورهای درون سوز و پیل های سوختی، روش های تولید آن، اثرات زیست محیطی و نقش آینده آن در چشم انداز انرژی نیز پرداخته می شود. در همین راستا، برای واحدهای صنعتی و پژوهشی که به تأمین مطمئن این سوخت نیاز دارند، انجام خرید متانول تهران یکی از رایج ترین و دسترس پذیرترین گزینه ها محسوب می شود، زیرا کیفیت مناسب و تأمین پایدار آن در عملکرد سیستم های انرژی بر اهمیت زیادی دارد.
ویژگی های شیمیایی سوخت متانول
متانول (CH₃OH) سادهترین نوع الکل است و یک مایع آلی قطبی محسوب می شود که ویژگی های شیمیایی آن بر رفتارش به عنوان سوخت تأثیرگذار است. متانول در دمای محیط یک مایع بی رنگ با بوی ضعیف الکلی است. جرم مولکولی پایینی دارد (۳۲ گرم بر مول) و نقطه جوش آن حدود ۶۵ °C است که نشان دهنده فراریت بالای آن می باشد و سبب میشود به راحتی تبخیر شده و برای احتراق آماده گردد. چگالی متانول در حدود ۰٫۷۹ گرم بر سانتیمتر مکعب (سبکتر از آب) است و در هر نسبتی با آب امتزاج پذیر است، به طوری که متانول و آب یک فاز یکنواخت تشکیل می دهند. این حلالیت در آب برای سوختی مایع غیرمعمول است و بر روش های اطفاء حریق تأثیر می گذارد، زیرا میتوان با رقیق کردن متانول در آب شعله آن را کنترل کرد. از نظر شیمیایی، مولکول متانول حاوی اکسیژن است (بر خلاف سوخت های هیدروکربنی خالص مانند بنزین) و این بدان معناست که از قبل تا حدی اکسید شده است. وجود این اکسیژن در ساختار مولکول باعث می شود محتوای انرژی متانول به ازای هر واحد جرم کمتر از سوخت های تماما هیدروکربنی باشد، اما در مقابل احتراق پاک تری با دوده بسیار کمتر ایجاد می کند. این مجموعه ویژگی ها، در کنار بررسی خواص شیمیایی متانول نشان می دهد که فراریت زیاد، امتزاج پذیری با آب، جرم مولکولی کم و حضور اکسیژن در ساختار، رفتار این ماده را به عنوان یک سوخت اشتعال پذیر و انرژی زا شکل می دهند.
ویژگی های اشتعال پذیری متانول
متانول جزو مواد فوق العاده قابل اشتعال است و در حضور منبع جرقه یا شعله به سادگی آتش می گیرد. نقطه اشتعال متانول حدود ۱۱ °C بالای صفر می باشد؛ یعنی در دمای کمی بالاتر از دمای اتاق می تواند به اندازه کافی بخار تولید کند تا با هوا مخلوط قابل اشتعالی تشکیل دهد. این نقطه اشتعال پایین باعث می شود متانول در رده مایعات بسیار آتش گیر قرار گیرد که در صورت عدم احتیاط، به راحتی آتش می گیرند. بخارات متانول به خوبی با هوا مخلوط می شوند و حتی ممکن است از محل انتشار خود فاصله گرفته و به یک منبع احتراق دور برسند. بخار متانول کمی از هوا سنگین تر است، بنابراین می تواند در نزدیکی سطح زمین یا در فضاهای بسته جمع شود و در حضور یک جرقه یا شعله مشتعل گردد. در صورت سوختن، متانول به سرعت می سوزد و گرما به همراه بخار آب و دی اکسید کربن آزاد می کند. به دلیل همین ویژگی های اشتعال پذیری، هنگام ذخیره سازی یا استفاده از متانول باید احتیاط های سختگیرانه ای رعایت شود؛ از جمله دور نگه داشتن آن از جرقه، شعله یا سطوح داغ و استفاده از تهویه مناسب برای پراکنده کردن بخاراتی که در غیر این صورت ممکن است ناگهان مشتعل شوند.
ویژگی های احتراق و حدود اشتعال متانول
رفتار اشتعال متانول با داشتن دمای خود آتش گیری نسبتاً بالا و محدوده اشتعال گسترده ای مشخص می شود. دمای خود آتش گیری متانول حدود ۴۶۴ °C است؛ یعنی باید تا دمای بسیار زیادی گرم شود تا بدون جرقه مستقیماً شعله ور گردد. این دما از دمای خود اشتعال بنزین بیشتر است و نشان می دهد که بخارات متانول نسبت به بنزین کمتر احتمال دارد صرفاً بر اثر تماس با سطوح داغ شعله ور شوند. با این حال در حضور یک منبع جرقه یا شعله، متانول برای آتش گرفتن به انرژی بسیار کمی نیاز دارد حتی یک جرقه ساکن کوچک می تواند بخار متانول را شعله ور کند. حدود اشتعال متانول در هوا تقریبا بین ۶٪ تا ۳۶٪ حجمی است. به عبارت دیگر، اگر بخار متانول بین حدود ۶٪ (حد پایین انفجار) تا ۳۶٪ (حد بالای انفجار) از حجم هوا را تشکیل دهد، یک شعله می تواند در این مخلوط منتشر شود. این بازه بسیار وسیع، نشان می دهد که متانول حتی در غلظت های نسبتاً کم در هوا یا در مخلوط های نسبتاً غنی از سوخت نیز قادر به سوختن است. این امر ضرورت کنترل دقیق نشت ها و تهویه مناسب را برجسته می کند، چرا که بخارات متانول می توانند در دامنه گسترده ای از غلظت ها همچنان قابل اشتعال باقی بمانند.
ملاحظات ایمنی در برابر آتش سوزی متانول
استفاده از متانول به عنوان سوخت مستلزم رعایت دقیق نکات ایمنی به دلیل رفتار خاص آن در زمان آتش سوزی است. یکی از مخاطرات قابل توجه این است که متانول با شعله آبی کمرنگ می سوزد که در روشنایی روز تقریباً نامریی است. به علت نبود درخشندگی قابل مشاهده، ممکن است آتش سوزی متانول فوراً تشخیص داده نشود و همین امر آن را خطرناک تر می کند زیرا افراد ممکن است متوجه نشوند که یک ناحیه در حال سوختن است. علاوه بر این، شعله متانول نسبت به شعله بنزین گرمای تابشی کمتری تولید می کند و فرد تا زمانی که بسیار به آتش نزدیک نشده باشد گرمای شدید را احساس نمی کند. این ترکیب از قابل رویت نبودن شعله و حرارت تابشی کمتر می تواند باعث تماس تصادفی افراد با آتش شود. برای افزایش ایمنی، گاهی از مواد افزودنی یا حسگرهای ویژه شعله استفاده می شود تا وجود آتش متانول را آشکار کنند. در زمینه اطفاء حریق، متانول چالش ها و البته مزایایی دارد: از آنجا که در آب حل می شود، می توان از آب برای رقیق سازی و کمک به خاموش کردن آتش های کوچک متانول استفاده کرد و با کاهش غلظت سوخت، مخلوط را از حالت قابل اشتعال خارج نمود. در مقابل، برای آتش های بزرگ ناشی از متانول معمولاً از فوم های مقاوم در برابر الکل یا خاموش کننده های شیمیایی خشک برای خفه کردن شعله استفاده می شود. نگهداری متانول باید در ظروف مخصوص مقاوم در برابر آتش و دارای تهویه مناسب انجام شود و مخازن باید برچسب گذاری واضحی داشته باشند. هر کسی که با متانول سروکار دارد باید آموزش دیده باشد تا به قابلیت اشتعال آن و نامحسوس بودن شعله های آن آگاه باشد و احتیاط لازم را به عمل آورد.
محتوای انرژی و ارزش حرارتی متانول
یکی از جنبه های مهم سوخت متانول میزان انرژی آن است که معمولاً با گرمای احتراق یا ارزش حرارتی بیان می شود. متانول حدود ۲۰ مگاژول انرژی به ازای هر کیلوگرم فراهم می کند بسته به پایین یا بالابودن ارزش حرارتی، این رقم میتواند بین حدود ۱۹٫۷ تا ۲۲٫۷ MJ/kg متغیر باشد. به عبارت عملی متانول حجماً تقریباً نصف انرژی بنزین را دارند. هر لیتر متانول حدود ۱۵٫۶ مگاژول انرژی آزاد می کند، در حالی که یک لیتر بنزین حدود ۳۲ مگاژول انرژی تولید می کند. این بدان معناست که برای دستیابی به همان خروجی انرژی، تقریباً دو برابر حجم سوخت متانول در مقایسه با بنزین مورد نیاز است. چگالی انرژی پایین تر متانول ناشی از ساختار شیمیایی آن است مولکول متانول قبلاً در ترکیب خود حاوی اکسیژن می باشد که به جرم سوخت اضافه می شود بدون اینکه انرژی قابل ملاحظه ای به آن بیفزاید. البته عدد اکتان بسیار بالای متانول اجازه می دهد موتورهایی که با این سوخت طراحی شده اند با نسبت تراکم بیشتری کار کنند و شاید بتوانند بخشی از انرژی را به شکل کارآمدتری استخراج نمایند. با این وجود، ارزش حرارتی کمتر یک چالش بنیادی محسوب می شود؛ هر وسیله ای که با متانول کار می کند باید حجم سوخت بیشتری را برای پیمودن مسافت مشابه حمل کند یا در غیر این صورت برد عملیاتی کوتاه تری خواهد داشت.
ویژگی های احتراق و آلایندگی متانول
متانول هنگام سوختن ویژگی های متمایزی از خود نشان می دهد که بر عملکرد و آلاینده های حاصل تأثیر می گذارد. سرعت پیشروی شعله متانول نسبتاً بالا است، به این معنا که مخلوط سوخت-هوا می تواند در موتور یا مشعل به سرعت و به طور کامل بسوزد. دمای شعله آدیاباتیک متانول در هوا حدود ۱۸۷۰ °C می باشد که کمی پایین تر از دمای شعله بنزین است و به تشکیل اکسیدهای نیتروژن (NOx) کمتری منجر می شود در مقایسه با احتراق با دمای بسیار بالای بنزین یا گازوئیل. یکی از مزیت های کلیدی متانول، پاکیزه بودن فرآیند سوختن آن است: متانول هیچ عنصری مثل گوگرد یا هیدروکربن های سنگین در ترکیب خود ندارد، بنابراین هنگام احتراق عملاً دی اکسید گوگرد تولید نمی کند و دوده (ذرات معلق کربنی) بسیار اندکی بر جای می گذارد. موتورهایی که با متانول کار می کنند دود سیاه به مراتب کمتری منتشر می سازند. محصولات اصلی احتراق متانول (در صورت کامل بودن فرآیند سوختن) شامل دی اکسید کربن (CO₂) و بخار آب هستند. البته احتراق ناقص متانول می تواند منجر به تولید مونوکسید کربن و فرمالدهید (یک آلدهید سمی) شود، بنابراین تنظیم دقیق موتور و نسبت سوخت به هوا برای جلوگیری از این موارد مهم است. در مجموع سوخت متانول تمایل دارد که آلایندگی خروجی کمتری از نظر دوده و برخی گازهای مضر داشته باشد و در مقایسه با سوخت های سنگین تر هیدروکربنی به بهبود کیفیت هوا کمک کند.
متانول در برابر بنزین: بازده انرژی و عملکرد
مقایسه متانول و بنزین تفاوت های مهمی را در بازده انرژی و کارایی موتور نشان می دهد. همان طور که گفته شد، محتوای انرژی متانول به ازای هر لیتر به طور قابل ملاحظه ای کمتر از بنزین است، که به این معنی است خودرویی که با متانول خالص کار می کند معمولاً مسافت پیموده شده کمتری به ازای هر لیتر سوخت خواهد داشت، زیرا باید سوخت بیشتری برای تولید توان مشابه بسوزاند. در عمل، باک یا سیستم تزریق سوخت باید تقریباً دو برابر حجم متانول را برای تولید قدرتی معادل بنزین به موتور برساند. با این حال، متانول مزایایی دارد که تا حدی کمبود چگالی انرژی آن را جبران می کنند. این سوخت دارای عدد اکتان فوق العاده بالا بیش از ۱۰۰ RON است و به موتورها اجازه می دهد با نسبت های تراکم یا فشار توربو شارژ بالاتری بدون احتراق کوبشی کار کنند. همچنین تبخیر متانول اثر خنک کنندگی زیادی دارد که چگالی هوای ورودی به سیلندر را افزایش می دهد و راندمان حجمی و توان خروجی موتور را بهبود می بخشد. مجموع این عوامل به این معناست که موتوری که برای سوخت متانول بهینه سازی شده باشد می تواند قدرتی قابل مقایسه و حتی گاهی بیشتر از موتور بنزینی تولید کند، albeit با مصرف سوخت بیشتر. از سوی دیگر، روشن کردن موتور با متانول در هوای سرد دشوارتر است، چون متانول گرمای تبخیر بالاتری دارد و در دمای پایین به اندازه بنزین به خوبی تبخیر و مشتعل نمی شود؛ در حالی که بنزین حتی در موتور سرد نیز به راحتی آتش می گیرد.
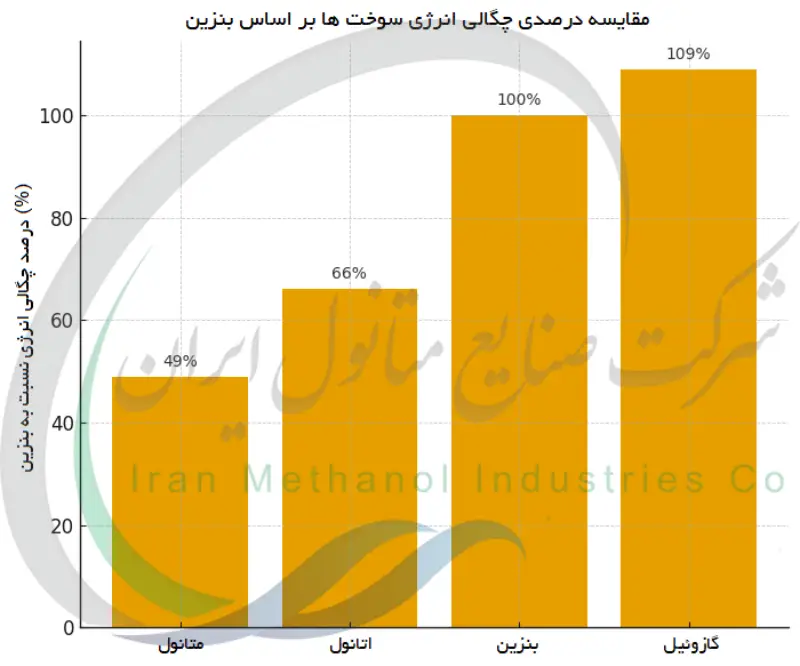
مقایسه ویژگی های متانول، اتانول، بنزین و گازوئیل
متانول و اتانول هر دو از خانواده الکل ها به شمار می روند، در حالی که بنزین و گازوئیل سوخت های هیدروکربنی حاصل از نفت هستند. مقایسه خواص آن ها دیدگاه روشنی در مورد تفاوت های اشتعال پذیری و انرژی این سوخت ها به دست می دهد. متانول و اتانول شباهت هایی با هم دارند: هر دوی آن ها مایعات فراری هستند که نقطه اشتعال پایینی دارند حدود ۱۱–۱۳ °C و در نتیجه به آسانی مشتعل می شوند. همچنین این دو سوخت دارای اکسیژن در ساختار مولکولی خود هستند که آن ها را در دسته سوخت های اکسیژنه قرار می دهد؛ حضور اکسیژن سبب می شود احتراقشان پاک تر باشد اما محتوای انرژی به ازای واحد جرم کمتری نسبت به سوخت های تمام هیدروکربنی داشته باشند. بنزین، که مخلوطی از هیدروکربن هاست، نقطه اشتعال فوق العاده پایینی (در حدود ۴۳- درجه سانتیگراد زیر صفر) دارد و در محدوده دمایی تقریباً ۳۰ تا ۲۰۰ °C به جوش می آید؛ به این معنی که حتی در شرایط بسیار سرد نیز بخارات قابل اشتعال آزاد می کند. گازوئیل به عنوان یک سوخت سنگین تر، نقطه اشتعال بالایی دارد معمولاً بیش از ۵۲ °C و در دمای محیط به سختی بخار کافی برای اشتعال آزاد می کند، اما تحت فشار و تراکم بالا در موتور دیزل یا در صورت گرم شدن می تواند مشتعل شود. از نظر بازده انرژی، بنزین و گازوئیل انرژی به مراتب بیشتری به ازای هر کیلوگرم و هر لیتر نسبت به متانول یا اتانول دارند؛ این امر به مسافت پیمایش یا توان بیشتر به ازای واحد سوخت منجر می شود. به طور مثال اتانول تقریباً دو سوم انرژی بنزین در هر لیتر را دارد و متانول حدود نیمی از انرژی بنزین را و به همین دلیل برای یک خروجی انرژی یکسان حجم بیشتری از این سوخت های الکلی مورد نیاز است. جدول زیر برخی از ویژگی های کلیدی متانول، اتانول، بنزین و گازوئیل را برای مقایسه خلاصه کرده است:
| ویژگی | متانول (CH₃OH) | اتانول (C₂H₅OH) | بنزین | گازوئیل (دیزل) |
|---|---|---|---|---|
| فرمول شیمیایی | CH₃OH | C₂H₅OH | مخلوط هیدروکربنی C₄–C₁₂ | مخلوط هیدروکربنی C₁₂–C₂₀ |
| نقطه جوش (°C) | ۶۴٫۷°C | ۷۸°C | ۳۰–۲۰۰°C (بازه) | ۱۵۰–۳۷۰°C (بازه) |
| نقطه اشتعال (°C) | ۱۱°C | ۱۳°C | -۴۳°C | ~۵۲°C |
| دمای خود آتش گیری (°C) | ~۴۶۴°C | ~۳۶۳°C | ~۲۶۰°C | ~۲۱۰°C |
| حدود اشتعال (٪ حجمی) | ۶–۳۶٪ | ۳٫۳–۱۹٪ | ۱٫۴–۷٫۶٪ | ۰٫۶–۷٪ |
| محتوای انرژی (مگاژول/کیلوگرم) | ~۲۰ مگاژول/کیلوگرم | ~۲۷ مگاژول/کیلوگرم | ~۴۴ مگاژول/کیلوگرم | ~۴۲ مگاژول/کیلوگرم |
| چگالی انرژی (مگاژول/لیتر) | ~۱۵٫۸ مگاژول/لیتر | ~۲۱ مگاژول/لیتر | ~۳۲ مگاژول/لیتر | ~۳۵ مگاژول/لیتر |
| چگالی (گرم/سانتیمتر³ در ۲۰°C) | ۰٫۷۹ گرم/سانتیمتر³ | ۰٫۷۹ گرم/سانتیمتر³ | ~۰٫۷۴ گرم/سانتیمتر³ | ~۰٫۸۴ گرم/سانتیمتر³ |
متانول در موتورهای درون سوز
متانول به دلیل خصوصیات احتراقی مناسبش در موتورهای احتراق داخلی (به ویژه در کاربردهای مسابقه ای و با عملکرد بالا) به کار گرفته شده است. عدد اکتان بسیار بالا در متانول به موتور اجازه می دهد با نسبت تراکم زیاد یا فشار توربوشارژ بالا کار کند که می تواند توان خروجی بیشتری ایجاد نماید. همچنین گرمای تبخیر بالای متانول باعث خنک شدن قابل توجه مخلوط هوا-سوخت هنگام تبخیر می شود و مانند یک افترکولر داخلی عمل کرده و هوای متراکم تر و غنی تری را وارد سیلندر می کند. سری مسابقاتی نظیر ایندی کار برای دهه ها از سوخت متانول استفاده می کردند, چرا که توان بالایی فراهم مینمود و از نظر ایمنی نیز مناسب بود (آتش متانول را می توان با آب کنترل کرد). در مسابقات درگ نیز متانول به دلیل پتانسیل توان بالایش همچنان محبوب است. البته استفاده از متانول در موتورهای استاندارد نیازمند برخی اصلاحات است. از آنجا که متانول حاوی اکسیژن است و نسبت شیمیایی سوخت به هوا در آن متفاوت از بنزین می باشد، سیستم سوخت رسانی باید تقریباً دو برابر سوخت بیشتر تزریق کند تا مخلوط رقیقی ایجاد نشود. انژکتورهای بزرگ تر یا ژیگلورهای کاربراتور با اندازه بزرگ تر برای جلوگیری از فقیر شدن مخلوط لازم است. همچنین، متانول می تواند به برخی فلزات (مثل آلومینیوم) خوردگی وارد کند و به برخی قطعات لاستیکی آسیب برساند، بنابراین جنس قطعات سیستم سوخت باید با آن سازگار باشد. اگرچه متانول خالص (M100) به طور گسترده در خودروهای سواری استفاده نشده است، برخی خودروهای انعطاف پذیر از نظر سوخت (Flex-Fuel) و برنامه های آزمایشی نشان داده اند که می توان موتورهایی را طراحی کرد که با متانول یا مخلوط های متانول-بنزین کار کنند.
پیل های سوختی مستقیم متانول و بازده آنها
متانول را می توان مستقیماً در دستگاه هایی به نام پیل سوختی مستقیم متانول Direct Methanol Fuel Cell یا DMFC برای تولید برق به کار گرفت. در یک پیل سوختی متانولی مستقیم، متانول به همراه آب در آند وارد پیل شده و در آنجا یک واکنش الکتروشیمیایی رخ می دهد که حاصل آن تولید دی اکسید کربن، یون های هیدروژن (H^+) و الکترون است. الکترون ها از طریق مدار خارجی جریان یافته و توان الکتریکی ایجاد می کنند، در حالی که یون های H^+ از میان غشا به سمت کاتد عبور می کنند و در آنجا با اکسیژن ترکیب شده و آب تشکیل می دهند. این فرآیند انرژی شیمیایی متانول را بدون احتراق مستقیماً به الکتریسیته تبدیل می کند. بازده (کارایی) کلی پیل های سوختی مستقیم متانول معمولاً در محدوده ۲۰٪ تا ۳۰٪ است که پایین تر از بازده پیل های سوختی هیدروژنی می باشد؛ بخشی از این تفاوت به خاطر مشکلاتی مانند عبور متانول از غشا (بدون واکنش) و سرعت پایین تر واکنش های الکتروشیمیایی است. با این حال، DMFC ها یک مزیت بزرگ دارند و آن قابلیت استفاده از یک سوخت مایع پرانرژی است که ذخیره و حمل آن در مقایسه با گاز هیدروژن فشرده آسان تر است. از این پیل ها در مواردی نظیر بسته های توان قابل حمل، تجهیزات نظامی و برخی خودروهای آزمایشی استفاده شده است. روش دیگر این است که متانول را به عنوان حامل هیدروژن به کار ببرند: متانول می تواند در داخل وسیله نقلیه به هیدروژن تبدیل (ریفورم) شده و سپس در یک پیل سوختی معمولی هیدروژنی استفاده شود. این روش، راحتی سوخت مایع را با بازده بیشتر پیل سوختی هیدروژنی ترکیب می کند.
روش های تولید متانول و منابع انرژی
متانول به صورت صنعتی از روش ها و خوراک های مختلفی تولید می شود که هر کدام مشخصات انرژی ویژه خود را دارند. روش معمول امروز استفاده از گاز طبیعی به عنوان ماده اولیه است؛ در این فرآیند ابتدا با استفاده از بخار آب، گاز طبیعی را به گاز سنتز (مخلوط هیدروژن و مونوکسید کربن) تبدیل می کنند و سپس با کمک کاتالیزور این گاز به متانول (CH₃OH) تبدیل می شود. این فرآیند انرژی بر است اما به خوبی تثبیت شده و در واقع انرژی شیمیایی نهفته در گاز طبیعی را با مقداری تلفات به صورت سوخت مایع متانول درمی آورد. متانول همچنین می تواند از زغال سنگ از طریق گازسازی یا از زیست توده به روش های مشابه تولید شود، اگرچه این مسیرها پرهزینه تر یا پیچیده تر هستند. رویکرد نوظهوری که اهمیت زیادی یافته است، تولید متانول از منابع تجدیدپذیر است: مثلاً گرفتن دی اکسید کربن (CO₂) از خروجی کارخانه ها یا هوا و ترکیب آن با هیدروژنی که از برق تجدیدپذیر (الکترولیز آب) به دست آمده است. حاصل این ترکیب، متانول سبز است که ردپای کربن بسیار کمتری دارد و عملاً انرژی برق تجدیدپذیر را در قالب یک سوخت شیمیایی ذخیره می کند. منبع انرژی مورد استفاده برای تولید متانول تأثیر زیادی بر پایداری آن دارد متانولی که از سوخت های فسیلی ساخته می شود، کربن همان سوخت ها را در خود دارد، در حالی که متانولی که از CO₂ و هیدروژن تجدیدپذیر سنتز شود تقریباً کربن خنثی خواهد بود. گوناگونی مسیرهای تولید بدان معناست که متانول را می توان در هر جایی که منبعی از کربن و انرژی وجود داشته باشد تولید کرد و این انعطاف پذیری، توان تأمین سوخت را در زنجیره انرژی افزایش می دهد.





بررسی نقطه اشتعال و محدوده اشتعال پذیری متانول و راهکارهای کاهش خطر آتش سوزی ناشی از این ماده
بررسی حرارت احتراق متانول و مقدار انرژی سوختی آن و آینده این ماده به عنوان منبع انرژی و سوخت جایگزین
بررسی محصولات احتراق متانول و جایگاه این ماده در آینده سوخت های پاک
بررسی مفهوم انرژی سوخت و مقایسه میزان انرژی متانول با بنزین و گازوئیل