فهرست عناوین
- مقدمه
- مروری بر متانول و کاربردهای رایج آن
- ویژگی های فیزیکی و شیمیایی متانول
- وجود متانول در طبیعت و محیط زیست
- جذب و متابولیسم متانول در بدن
- سازوکار سمیت متانول (فرمالدهید و اسید فرمیک)
- اثرات سمی حاد و علائم
- آسیب عصب بینایی و نابینایی
- دوز مرگبار، حدود مواجهه و آستانه های خطر
- مواجهه مزمن و اثرات بلندمدت
- تشخیص مسمومیت با متانول
- درمان و پادزهرها
- منابع مسمومیت با متانول (تصادفی و عمدی)
- اقدامات ایمنی و پیشگیری
- مقایسه سمیت متانول و اتانول
نوشته شده توسط شرکت صنایع متانول ایران
منتشر شده توسط شرکت صنایع متانول ایران
تاریخ انتشار مقاله : 09-09-1404
تاریخ بروزرسانی مقاله : 09-09-1404
تعداد کلمات : 3800
آدرس مقاله : لینک مقاله
خواص سمی و بیولوژیکی متانول

مقدمه
متانول یک الکل ساده اما خطرناک است که به تاثیرات سمی آن بر موجودات زنده شناخته میشود. متانول (که الکل چوب نیز نامیده میشود) کوچک ترین عضو خانواده الکل ها است و به طور گسترده به عنوان یک ماده شیمیایی صنعتی و سوخت استفاده میشود. این مایع بی رنگ و فرار دارای بوی ملایم الکلی است. با وجود کاربرد وسیع آن، متانول حتی در دوزهای کم میتواند برای انسان ها و حیوانات به شدت سمی باشد. هنگام نوشیدن، استنشاق یا جذب از طریق پوست، متانول میتواند مشکلات جدی سلامتی ایجاد کند. در بدن، متانول به ترکیبات سمی متابولیزه میشود که بر سیستم عصبی و اندام ها تاثیر میگذارند. در بخش های بعدی ویژگی های شیمیایی متانول، نحوه متابولیزه شدن آن، سازوکار سمیت آن، علائم مسمومیت و اثرات ماندگار آن بر سلامت را بررسی خواهیم کرد. همچنین درباره روش های ایمن کار با متانول، تاثیر آن بر محیط زیست، و مقایسه سمیت متانول با الکل آشناتر یعنی اتانول بحث خواهیم کرد.
مروری بر متانول و کاربردهای رایج آن
متانول یک ماده شیمیایی است که به طور گسترده تولید می شود و کاربردهای زیادی در صنایع مختلف دارد. این ماده از گاز طبیعی یا زیست توده سنتز می شود و به عنوان بلوک سازنده برای محصولات متعددی عمل می کند. متانول به عنوان یک حلال صنعتی و ماده اولیه، برای تولید فرمالدهید، اسید استیک، پلاستیک ها و سایر مواد شیمیایی استفاده می شود. همچنین به عنوان یک سوخت با اکتان بالا یا افزودنی سوخت در برخی موتورها و در تولید بیودیزل کاربرد دارد. متانول که به طور تاریخی به عنوان الکل چوب شناخته می شود، در محصولاتی مانند ضدیخ، مایع شیشه شوی خودرو، تینر رنگ و محلول های پاک کننده صنعتی یافت می شود و در آزمایشگاه ها نیز یک حلال رایج است. برخلاف اتانول (الکل نوشیدنی)، متانول برای مصرف انسانی مناسب نیست زیرا بسیار سمی است و مصرف اشتباه آن می تواند منجر به مسمومیت شدید شود. به همین دلیل شناخت محل های مصرف متانول، کاربردها و خطرات احتمالی آن برای جلوگیری از بروز حوادث اهمیت بالایی دارد. سالانه میلیون ها تن متانول در جهان تولید می شود که نشان دهنده جایگاه آن به عنوان یک ماده شیمیایی کالایی مهم است. حضور گسترده این ماده سبب می شود افراد و صنایع در خرید و مصرف آن دقت کافی داشته باشند. به همین دلیل انتخاب منابع معتبر مانند خرید متانول کارون می تواند نقش مهمی در استفاده ایمن و استاندارد از این ماده شیمیایی داشته باشد.
ویژگی های فیزیکی و شیمیایی متانول
ویژگی های فیزیکی و شیمیایی متانول مبنای رفتار آن در سیستم های زیستی و محیط هستند. متانول خالص یک مایع شفاف و بی رنگ است که شبیه آب به نظر می رسد و بوی ملایم شبیه به الکل دارد. این ماده بسیار آتش گیر است و با شعله آبی تقریبا نامرئی در هوا می سوزد. درک دقیق قابلیت اشتعال و انرژی زایی متانول اهمیت زیادی دارد، زیرا همین ویژگی ها آن را به ماده ای حساس و نیازمند مدیریت ایمن تبدیل می کنند. نقطه جوش متانول حدود ۶۵ درجه سانتیگراد است و بهراحتی با آب و بسیاری از حلالهای آلی مخلوط میشود. از نظر شیمیایی، فرمول CH3OH آن نشان دهنده ساختار تک کربنه با یک گروه OH است که آن را ساده ترین الکل می سازد. این ساختار ساده به متانول اجازه می دهد به راحتی از غشاهای زیستی عبور کند. چگالی متانول حدود ۰.۷۹ گرم بر میلی لیتر است که کمی سبک تر از آب است. به دلیل ظاهر و بوی مشابه با اتانول، ممکن است افراد متانول را به اشتباه بنوشند بدون اینکه خطر آن را متوجه شوند. متانول در محلول قطبی است و می تواند بسیاری از مواد را حل کند، به همین دلیل به عنوان یک حلال صنعتی ارزشمند است. این ویژگی ها همچنین باعث می شوند متانول در بدن انسان به سرعت جذب شود و سریعا توزیع گردد. فراریت متانول نیز به خطرات استنشاقی آن کمک می کند، زیرا می تواند تبخیر شود و در محیط های با تهویه ضعیف به صورت بخار استنشاق گردد.
وجود متانول در طبیعت و محیط زیست
متانول نه تنها یک محصول صنعتی است، بلکه در طبیعت نیز به مقدار کم وجود دارد. بسیاری از میوه ها و سبزیجات به طور طبیعی متانول با غلظت ناچیز دارد که حاصل تجزیه پکتین است و نوشیدنی های تخمیری دارای سطوح بسیار کوچکی از متانول هستند که برای ایجاد آسیب بسیار ناچیز است. بدن انسان می تواند این مقادیر جزئی را بدون اثر منفی پردازش کند. حتی گیاهان هم متانول را در هوا آزاد می کنند، بنابراین انسان ها روزانه مقادیر بسیار ناچیزی از متانول را از منابع طبیعی استنشاق یا مصرف می کنند. متانول همچنین می تواند از برخی افزودنی های غذایی نشأت بگیرد؛ به عنوان مثال شیرین کننده مصنوعی آسپارتام هنگام متابولیزه شدن مقدار بسیار کمی متانول آزاد می کند که بسیار پایین تر از هر سطح سمی است. انتشارهای محیطی متانول، مانند ریزش ها، معمولا برای مدت طولانی باقی نمی مانند. متانول به راحتی تجزیه زیستی می شود، زیرا میکروب های خاک و آب آن را در مدت کوتاهی به دی اکسید کربن و آب تجزیه می کنند. در حالی که یک نشت با غلظت بالا می تواند به طور موقت به حیات وحش یا آبزیان آسیب برساند، متانول عموما خیلی سریع تر از بسیاری از مواد شیمیایی دیگر پخش می شود و از بین می رود. به طور کلی در زندگی روزمره ما تنها با مقادیر ناچیز و غیر سمی متانول مواجه می شویم و این ماده به دلیل تجزیه سریع خود در محیط تجمع نمی یابد.
جذب و متابولیسم متانول در بدن
متانول می تواند از راه خوردن، استنشاق یا حتی جذب پوستی وارد بدن شود و سریعا توسط جریان خون جذب می گردد. پس از ورود، در تمام آب فضای بدن پخش می شود و به تمام اندام ها و بافت ها می رسد. چون در تمام آب بدن مخلوط می شود و به طور قابل توجهی به پروتئین ها متصل نمی شود، متانول به راحتی به اندام هایی مانند مغز و چشم می رسد. جذب از معده سریع است غلظت خونی در عرض حدود یک ساعت پس از خوردن به اوج می رسد و بخارات استنشاقی متانول نیز به راحتی از طریق ریه وارد گردش خون می شوند. سپس کبد متانول را طی مراحل متوالی متابولیزه می کند: یک آنزیم (الکل دهیدروژناز) ابتدا متانول را به فرمالدهید تبدیل می کند و آنزیم دیگر (آلدهید دهیدروژناز) فرمالدهید را سریعا به اسید فرمیک (فرمات) تبدیل می کند. این فرایند متانول نسبتا بی ضرر را به ترکیبات بسیار سمی تری تبدیل می کند. مقداری از متانول که متابولیزه نشده باقی مانده است نیز بدون تغییر از طریق هوای بازدم و ادرار دفع می شود. قابل ذکر است که تجزیه متانول در بدن کندتر از اتانول است. در نتیجه، متانول مدت بیشتری در سیستم بدن باقی می مانند و می تواند به تولید متابولیت های سمی برای مدت طولانی ادامه دهد. درک این فرآیند جذب و متابولیسم برای شناخت چگونگی تجمع سطوح سمی متانول و فرآورده های آن در بدن پس از تماس، کلیدی است.
سازوکار سمیت متانول (فرمالدهید و اسید فرمیک)
اثرات خطرناک متانول ناشی از خود ترکیب نیست بلکه از متابولیت های آن است. متانول در ابتدا اثر تضعیف کننده خفیفی بر سیستم عصبی مرکزی دارد (مشابه اتانول)، اما تهدید واقعی زمانی آغاز می شود که بدن آن را به فرمالدهید و سپس به اسید فرمیک متابولیزه می کند. فرمالدهید ترکیبی بسیار واکنش پذیر اما کوتاه عمر است، زیرا سریعا به اسید فرمیک تبدیل می شود. اسید فرمیک (فرمات) بسیار سمی است باعث اسیدوز متابولیک (اسیدی شدن بیش از حد خون) می شود و همچنین در توانایی سلول ها برای استفاده از اکسیژن اختلال ایجاد می کند. به طور مشخص، فرمات یک آنزیم کلیدی در میتوکندری (سیتوکروم اکسیداز) را مهار می کند و تولید انرژی را متوقف کرده و منجر به هیپوکسی سلولی (محرومیت سلول از اکسیژن) به ویژه در بافت های حساس می شود. سلول های عصبی به خصوص آسیب پذیر هستند؛ عصب بینایی چشم اغلب هدف اصلی سمیت فرمات است، که نابینایی مرتبط با مسمومیت متانول را توضیح می دهد. ترکیب اسیدوز شدید و کمبود اکسیژن سلولی می تواند در موارد بحرانی به نارسایی چند اندام منجر شود. در واقع، متانول اگر در بدن به این سموم تبدیل نمی شد نسبتا بی خطر بود. درک این سازوکار مهم است و درمان های مسمومیت با متانول بر مسدود کردن تشکیل آن متابولیت های سمی تمرکز دارند.
اثرات سمی حاد و علائم
مسمومیت حاد با متانول تمایل دارد به صورت مراحلی پیشرفت کند. در ابتدا، فرد ممکن است تنها علائم خفیف و غیراختصاصی داشته باشد مانند سردرد، سرگیجه, تهوع و کمی خواب آلودگی اثراتی که شاید شبیه مستی خفیف ناشی از الکل باشند. اثرات اولیه متانول بر سیستم عصبی مرکزی اغلب کمتر از اثرات اتانول است، که می تواند افراد را به کم اهمیت دانستن خطر گمراه کند. پس از این علائم اولیه، معمولا دوره پنهانی چند ساعت بدون علائم واضح وجود دارد در حالی که متانول در حال متابولیزه شدن است. به محض اینکه متابولیت های سمی به اندازه کافی جمع شوند، علائم شدید ظاهر می شوند، معمولا ۱۲ تا ۲۴ ساعت پس از مواجهه (زودتر اگر دوز بسیار زیادی مصرف شده باشد). یکی از علائم شاخص اختلال بینایی است: تاری یا تیره شدن دید که اغلب به صورت دیدن طوفان برفی توصیف می شود, همراه با حساسیت به نور. با توسعه اسیدوز متابولیک، ممکن است فرد برای جبران اسیدوز شروع به تنفس سریع کند. دیگر علائم وخیم شونده شامل استفراغ، درد شکم و کم آبی بدن است. اگر درمان نشود، مسمومیت متانول می تواند به کما, تشنج و در نهایت مرگ بر اثر نارسایی تنفسی یا شوک منجر شود. این شروع تاخیری علائم تهدید کننده زندگی از مشخصه های سمیت متانول است و ضروری می سازد که بلافاصله پس از هر مواجهه مشکوک، کمک پزشکی گرفته شود حتی اگر فرد در ابتدا احساس خوبی داشته باشد.
آسیب عصب بینایی و نابینایی
مسمومیت با متانول به خاطر اثر آن بر چشم ها بدنام است به طور مشخص آسیب به اعصاب بینایی که می تواند باعث کوری جزئی یا کامل شود. مشکلات بینایی اغلب با تاری دید یا لکه هایی در میدان دید شروع می شوند و می توانند به سرعت به حالت طوفان برفی (دیدن مه سفید یا الگوهای شبیه برف) پیشرفت کنند. این اتفاق می افتد زیرا اسید فرمیک تجمع یافته از متابولیسم متانول به بافت عصب بینایی حمله می کند. دیسک بینایی (جایی که عصب بینایی وارد چشم می شود) ممکن است متورم شود و الیاف عصبی دچار آسیب می شود. اگر درمان به تاخیر بیفتد، این آسیب عصب بینایی می تواند دائمی شود و فرد را حتی پس از رفع سایر علائم نابینا باقی بگذارد. قابل توجه اینکه خوردن تنها چند میلی لیتر متانول (مثلا فقط یک یا دو قاشق چایخوری) می تواند برای آسیب غیرقابل برگشت به عصب بینایی کافی باشد. دلیل اینکه اعصاب بینایی این قدر آسیب پذیر هستند نیاز انرژی بالای آنها است اختلال فرمات در فرآیندهای انرژی سلولی این اعصاب را از انرژی محروم می کند و باعث از کار افتادن آنها می شود. حتی نجات یافتگان که از نابینایی کامل اجتناب می کنند ممکن است پس از بهبودی دچار نقص های ماندگار بینایی یا کاهش حدت بینایی شوند. احتمال قوی نابینایی ناشی از مسمومیت متانول این وضعیت را یک اورژانس پزشکی واقعی می سازد که نیاز به درمان فوری در اولین ظن دارد.
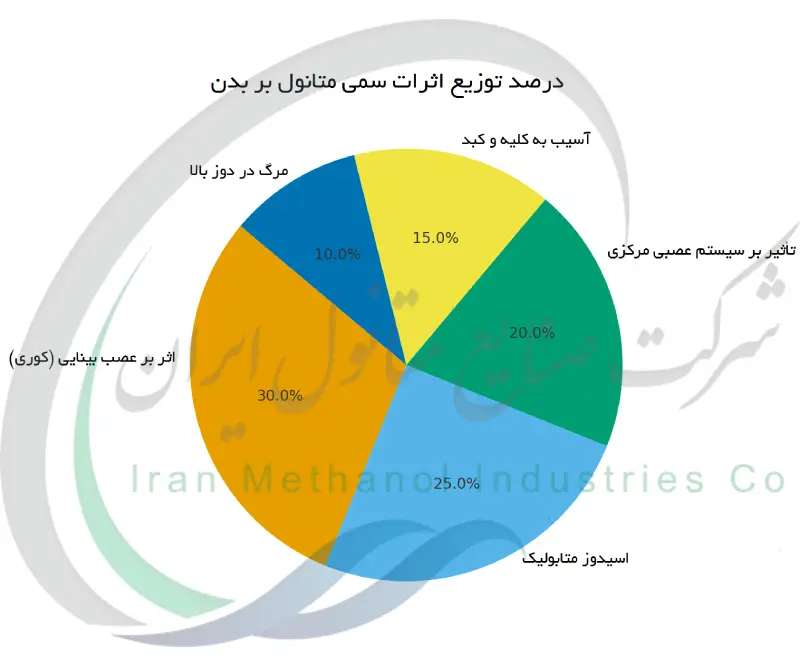
دوز مرگبار، حدود مواجهه و آستانه های خطر
متانول به مراتب قوی تر از اتانول به عنوان یک ماده سمی است و فقط مقدار کمی از آن می تواند کشنده باشد. دوز مرگبار تخمینی متانول برای یک بزرگسال متوسط حدود ۳۰ تا ۱۰۰ میلی لیتر (تقریبا معادل یک تا سه شات) متانول خالص است. در بسیاری از موارد گزارش شده، فقط ۳۰ میلی لیتر (حدود دو قاشق غذاخوری) متانول ۱۰۰٪ کافی بوده است تا در صورت تأخیر در درمان باعث مرگ شود. حتی مقادیر بسیار کمتر از حد کشنده می تواند آسیب جدی ایجاد کند: حدود ۱۰ میلی لیتر متانول ممکن است در صورت عدم درمان باعث کوری دائمی شود. از نظر وزن بدن، تقریبا ۳۰۰ تا ۱۰۰۰ میلی گرم متانول به ازای هر کیلوگرم می تواند کشنده باشد. در مقایسه، حجم کشنده اتانول برای یک بزرگسال بسیار بیشتر است (چند صد میلی لیتر اتانول خالص). برای حفاظت مردم از مواجهه تصادفی، دستورالعمل های ایمنی وجود دارد. مثلا در هوا محیط کار حد مجاز بخار متانول معمولا حدود ۲۰۰ قسمت در میلیون در یک شیفت ۸ ساعته تعیین شده است تا از خطرات مواجهه مزمن جلوگیری شود. همچنین یک مقدار مصرف روزانه ایمن (دوز مرجع) تنها ۰.۵ میلی گرم به ازای هر کیلوگرم وزن بدن تعیین شده است که نشان می دهد حتی مقادیر متوسط نیز ناایمن در نظر گرفته می شوند. همه این ارقام تاکید می کنند که فقط یک دوز بسیار کوچک متانول برای ایجاد مسمومیت شدید کافی است و به همین دلیل کار کردن با احتیاط و واکنش سریع به هرگونه مواجهه با متانول از اهمیت بالایی برخوردار است.
مواجهه مزمن و اثرات بلندمدت
مواجهه مزمن با دوز بالای متانول غیرمعمول است، اما مواجهه مداوم با دوز پایین یا عواقب مسمومیت حاد همچنان می توانند مشکلات ماندگاری ایجاد کنند. کارگرانی که به طور منظم بخارات متانول را تنفس می کنند (مثلا در کارخانه های با تهویه نامناسب) از سردردهای مداوم، سرگیجه، خستگی یا سوزش چشم به طور مداوم گزارش داده اند نشانه هایی که حتی دوزهای کوچک در طول زمان می توانند بر سیستم عصبی تاثیر بگذارند و اندام های حسی را تحریک کنند. از جنبه مثبت، مشخص نشده است که متانول باعث سرطان یا نقص ژنتیکی در انسان شود. اما نجات یافتگان از مسمومیت شدید متانول اغلب عواقب بلندمدتی را متحمل می شوند. نابینایی جزئی یا کامل دائمی در نجات یافتگان شایع است. برخی نیز دیگر مشکلات عصبی مانند لرزش یا مشکلات حرکتی شبیه پارکینسون را به دلیل آسیب مغزی (برای مثال، آسیب به گانگلیون های پایه مغز) توسعه می دهند. مشکلات شناختی از جمله از دست دادن حافظه یا هماهنگی ضعیف نیز گزارش شده است. برخلاف فلزات سنگین یا برخی مواد شیمیایی، متانول در طول سالیان در بدن تجمع نمی یابد؛ به محض قطع مواجهه، از بدن حذف می شود. اما حتی اگر متانول تجمع پیدا نکند، مواجهه مداوم بالاتر از سطوح ایمن هنوز هم می تواند به اثرات جزئی سلامت مداوم منجر شود. نکته مهم این است که هر گونه مواجهه با متانول باید تا حد ممکن کم نگه داشته شود تا هم از آسیب فوری و هم بلندمدت جلوگیری شود.
تشخیص مسمومیت با متانول
تشخیص سریع مسمومیت با متانول حیاتی است، اما می تواند دشوار باشد زیرا علائم اولیه آن تقلید سایر بیماری ها است. اولین گام جمع آوری هر گونه سرنخ از مواجهه است – برای مثال، شواهدی که کسی مایع مشکوکی نوشیده یا با حلال ها کار می کرده است. پزشکان به دنبال الگوی خاصی از یافته ها هستند: اسیدوز متابولیک (اسیدی شدن خون) همراه با اختلالات بینایی به شدت به متانول اشاره دارد. در آزمایش خون، اسیدوز متابولیک با آنیون گپ بالا یک ویژگی کلاسیک مسمومیت با متانول است. علاوه بر این، افزایش گپ اسمزی (که نشان دهنده وجود ماده نامشخصی در خون است) می تواند به سمت متانول یا یک الکل سمی دیگر اشاره کند. مطمئن ترین راه تشخیص، اندازه گیری سطح متانول در خون است، اما همه آزمایشگاه ها نمی توانند این آزمایش را سریعا انجام دهند، بنابراین پزشکان اغلب مجبورند بر اساس تشخیص احتمالی قبل از تایید عمل کنند. اغلب تشخیص بر اساس علائم بالینی و سرنخ های آزمایشگاهی انجام می شود پیش از آنکه نتایج تأییدی در دسترس باشند. معاینه چشم نیز می تواند شواهدی فراهم کند: تورم دیسک بینایی در بیماری با سابقه و علائم مرتبط، از مسمومیت متانول حمایت می کند. حتی یک بیمار بیهوش با اسیدوز غیرقابل توجیه فرض بر این گذاشته می شود که ممکن است مسمومیت با متانول داشته باشد و پزشکان بلافاصله درمان را به عنوان اقدام احتیاطی آغاز می کنند. شناخت زودهنگام این وضعیت بسیار مهم است، زیرا پادزهرها بهترین اثر را دارند اگر قبل از بروز اثرات شدید (مانند آسیب برگشت ناپذیر بینایی) تجویز شوند.
درمان و پادزهرها
درمان سریع پزشکی برای مسمومیت با متانول برای نجات جان و جلوگیری از آسیب دائمی (مانند کوری) ضروری است. رویکرد اصلی این است که از متابولیزه شدن متانول به محصولات سمی آن جلوگیری شود. این کار با دادن پادزهری که آنزیم الکل دهیدروژناز را مسدود می کند، انجام می شود. پادزهر ترجیحی فومپیزول است که مستقیما آنزیم را مهار می کند و در نتیجه از تبدیل متانول به فرمالدهید و اسید فرمیک جلوگیری می کند. اگر فومپیزول در دسترس نباشد، اتانول (الکل نوشیدنی معمولی) به عنوان پادزهر جایگزین استفاده می شود، زیرا اتانول برای همان آنزیم رقابت می کند و از این طریق متابولیسم متانول را کند می کند. در شرایط اورژانس، اتانول به صورت وریدی تزریق می شود تا آنزیم را اشباع کند. همودیالیز (تصفیه مکانیکی خون) نیز اغلب به کار گرفته می شود. دیالیز به سرعت متانول و فرمات را از جریان خون حذف می کند و همچنین به اصلاح اسیدوز متابولیک کمک می کند. مراقبت حمایتی شامل سدیم بی کربنات (برای کنترل اسیدوز) و اسید فولینیک (برای کمک به سم زدایی اسید فرمیک به دی اکسید کربن) نیز می شود. درمان ادامه می یابد تا زمانی که متانول حذف شود و تعادل اسید-باز خون به حالت عادی برگردد. با درمان سریع و تهاجمی، اکثر بیماران می توانند از مسمومیت با متانول جان سالم به در ببرند و از پیامدهای شدید جلوگیری کنند، به ویژه اگر درمان قبل از تجمع قابل توجه اسید فرمیک آغاز شود.
منابع مسمومیت با متانول (تصادفی و عمدی)
مسمومیت با متانول اغلب اتفاق می افتد زیرا قربانی ناآگاهانه آن را می نوشد یا چون متانول سر از مایعات قابل مصرف در می آورد. یک علت تصادفی رایج این است که متانول با الکل آشامیدنی اشتباه گرفته شود: برای مثال ممکن است کسی محصول حاوی متانول مانند مایع شیشه شوی خودرو یا ضد یخ را بنوشد، به ویژه اگر به طور نادرست در ظرف نوشیدنی نگهداری شده باشد. علت بزرگ دیگر بروز مسمومیت های جمعی، مشروبات الکلی تقلبی یا آلوده به متانول است. اگر مشروب در خانه بدون تکنیک های مناسب تقطیر شود یا عمدا با متانول ارزان مخلوط گردد، می تواند حاوی مقادیر خطرناک متانول باشد؛ موارد متعددی از مسمومیت های دسته جمعی ناشی از چنین نوشیدنی های تقلبی در سراسر جهان رخ داده است. متانول گاهی عمدا نیز نوشیده می شود: افراد برای خودکشی یا به دلیل وابستگی به الکل، متانول مصرف کرده اند (هنگامی که به جای نوشیدنی های الکلی معمولی، محصولاتی مانند الکل صنعتی یا سوخت را می نوشند) که پیامدهای وخیمی داشته است. جدا از بلعیدن، متانول می تواند از راه های دیگر نیز وارد بدن شود. استنشاق بخارات متانول در یک فضای کم تهویه (مثلا استفاده از آن به عنوان حلال در یک اتاق بسته) می تواند منجر به مسمومیت شود، همان طور که تماس پوستی قابل توجه (مثل ریختن مقدار زیاد آن روی پوست و جذب آن) نیز در صورت شسته نشدن متانول می تواند مسمومیت ایجاد کند. آگاهی از این منابع رایج مسمومیت با متانول برای پیشگیری حیاتی است.
اقدامات ایمنی و پیشگیری
پشگیری از مسمومیت با متانول مستلزم آموزش، مقررات و روش های ایمن هنگام کار با این ماده شیمیایی است. همه محصولاتی که حاوی متانول هستند باید با برچسب های هشدار خطر به وضوح مشخص شوند و هرگز نباید در بطری هایی که ممکن است با ظروف نوشیدنی اشتباه گرفته شوند نگهداری شوند. مردم باید بدانند که متانول جایگزین الکل نوشیدنی نیست حتی مقدار بسیار کمی از آن در صورت مصرف می تواند کشنده باشد. در محیط های شغلی، پروتکل های سختگیرانه ایمنی حیاتی هستند: تهویه مناسب برای جلوگیری از تجمع بخارات را فراهم کنید و از تجهیزات حفاظتی (دستکش، عینک) استفاده کنید زیرا متانول می تواند از طریق پوست جذب شود و چشم ها را تحریک کند. هر گونه نشت باید بلافاصله با تجهیزات حفاظتی مناسب تمیز شود. دولت ها همچنین قوانینی مانند افزودن مواد تلخ یا رنگ به محصولات حاوی متانول (مثلا ضد یخ) را برای جلوگیری از بلع تصادفی اجرا می کنند. مقابله با تولید الکل تقلبی (برای جلوگیری از نوشیدنی های آلوده به متانول) نیز راهبرد مهم دیگری است. برای افرادی که از متانول استفاده می کنند (مثلا به عنوان حلال یا سوخت در خانه)، اقدامات احتیاطی منطقی تاثیر زیادی دارد: کمترین مقدار لازم را استفاده کنید، آن را دور از دسترس کودکان نگه دارید، و تنها در ظروف دارای برچسب واضح نگهداری کنید. در نهایت، هوشیاری در هنگام کار با متانول و مقررات در هر دو سطح صنعتی و فردی می تواند میزان موارد مسمومیت با متانول را تا حد زیادی کاهش دهد.
مقایسه سمیت متانول و اتانول
متانول و اتانول هر دو الکل هستند، اما ویژگی های سم شناختی آنها به شدت متفاوت است. اتانول (الکلی که در نوشیدنی ها یافت می شود) و متانول (الکل چوب) ساختارهای مشابهی دارند، با این حال بدن آنها را به شکل متفاوتی پردازش می کند. اتانول می تواند مستی ایجاد کند و در دوزهای بیش از حد، عمدتا از طریق سرکوب سیستم عصبی مرکزی و تنفسی می تواند کشنده باشد. اما بدن اتانول را به استالدهید و سپس اسید استیک متابولیزه می کند که اگرچه در مقادیر بسیار زیاد مضر هستند، معمولا باعث نوع آسیب حاد اندامی که در مورد متانول دیده می شود نمی شوند. در مقابل، خود متانول مسمومیت اولیه کمتری ایجاد می کند، اما متابولیسم آن اسید فرمیک تولید می کند که منجر به اسیدوز متابولیک شدید و آسیب اختصاصی به اندام هایی مانند کوری می شود. به طور خلاصه، متانول از نظر سمیت حاد بسیار قوی تر از اتانول است. برای مثال، یک فرد می تواند مقدار متعادلی اتانول مصرف کند (اگرچه نوشیدن بیش از حد در طول زمان مضر است) اما تنها چند قاشق چایخوری متانول می تواند مسمومیت جدی ایجاد کند. جالب اینکه، اتانول به عنوان پادزهر برای مسمومیت متانول به کار می رود زیرا برای همان آنزیم متابولیک رقابت می کند و از تجزیه متانول به فرمات سمی جلوگیری می کند. جدول زیر تفاوت های کلیدی بین متانول و اتانول را از نظر سمیت و اثرات بیولوژیکی نشان می دهد:
| ویژگی | متانول (CH3OH) | اتانول (C2H5OH) | دوز سمی (تقریبی) | اثرات قابل توجه |
|---|---|---|---|---|
| ساختار شیمیایی | یک کربن (الکل چوب) | دو کربن (الکل غلات) | ندارد | متانول ساده ترین و کوچک ترین الکل است |
| کاربردهای معمول | حلال، سوخت، ضد یخ، ماده اولیه صنعتی | نوشیدنی ها (آبجو، شراب، لیکور)، حلال، افزودنی سوخت | ندارد | متانول برای نوشیدن نیست؛ اتانول الکل نوشیدنی است |
| محصول نهایی متابولیسم | اسید فرمیک (بسیار سمی) | اسید استیک (نسبتا بی ضرر) | ندارد | متابولیت های متانول باعث اسیدوز می شوند؛ متابولیت های اتانول در مقادیر کم چنین نیستند |
| حداقل حجم کشنده | حدود ۳۰ میلی لیتر (حدود ۲ قاشق غذاخوری) | حدود ۳۰۰ میلی لیتر (حدود ۱.۲۵ فنجان) | متانول: ۳۰ میلی لیتر؛ اتانول: ۳۰۰ میلی لیتر | متانول تقریبا ۱۰ برابر سمی تر از اتانول (بر حسب حجم) است |
| اثرات مقادیر کم | می تواند کوری و اسیدوز ایجاد کند (حتی حدود ۱۰ میلی لیتر خطرناک است) | مستی خفیف (نشئگی، اختلال قضاوت) | ۱۰ میلی لیتر متانول در مقابل ۱۰ میلی لیتر اتانول | سمیت متانول در دوزهایی ظاهر می شود که برای اتانول ناچیز است |
| پادزهر در مسمومیت | فومپیزول یا اتانول (مهار متابولیسم) | پادزهر خاصی ندارد؛ مراقبت حمایتی در اوردوز شدید | ندارد | خود اتانول برای درمان مسمومیت با متانول استفاده می شود |
| حد مجاز شغلی | حدود ۲۰۰ قسمت در میلیون در هوا (میانگین ۸ ساعت) | حدود ۱۰۰۰ قسمت در میلیون در هوا (میانگین ۸ ساعت) | ندارد | برای متانول حدود مجاز سختگیرانه تر است به دلیل سمیت بالاتر |
| اندام اصلی آسیب دیده | عصب بینایی (کوری)، اسیدوز متابولیک (آسیب چند اندام) | کبد (سیروز در مصرف مزمن)، سرکوب سیستم عصبی مرکزی در اوردوز حاد | ندارد | متانول مستقیما چشم ها و pH خون را هدف قرار می دهد؛ اتانول عمدتا در طول زمان به کبد آسیب می زند |





بررسی مکانیسم سمیت متانول در بدن و تفاوت متانول با اتانول
آشنایی با دوز کشنده متانول و علائم مسمومیت و بررسی تفاوت متانول با الکل های خوراکی از نظر سمیت
بررسی عوامل موثر بر شدت تاثیرات مزمن تماس با متانول بر سلامتی انسان