فهرست عناوین
- مقدمه
- ساختار شیمیایی و ترکیب متانول
- ویژگی های فیزیکی و ظاهر
- قطبیت و تشکیل پیوند هیدروژنی
- حلالیت و امتزاج پذیری
- قابلیت اشتعال و خواص احتراق
- سمیت و اثرات بر سلامتی
- رفتار اسیدی و بازی متانول
- واکنش های اکسیداسیون و محصولات جانبی
- تشکیل استر و اتر
- تبدیلات صنعتی و مشتقات متانول
- متانول به عنوان سوخت
- متانول به عنوان حلال در صنعت
- مقایسه با اتانول و سایر الکل ها
نوشته شده توسط شرکت صنایع متانول ایران
منتشر شده توسط شرکت صنایع متانول ایران
تاریخ انتشار مقاله : 28-08-1404
تاریخ بروزرسانی مقاله : 28-08-1404
تعداد کلمات : 3300
آدرس مقاله : لینک مقاله
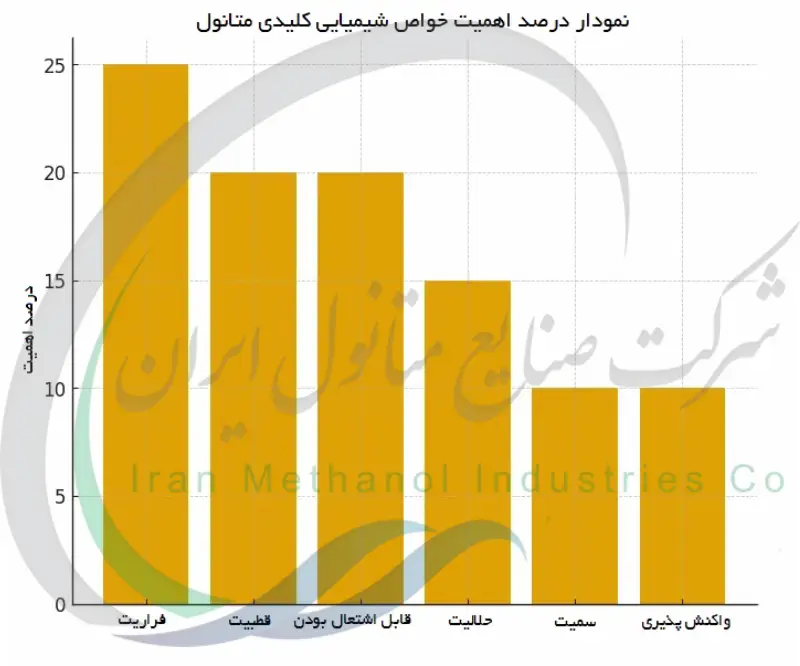
خواص شیمیایی متانول

مقدمه
متانول ساده ترین الکل است فرمول شیمیایی CH3OH که با نام های الکل متیلیک و الکل چوب نیز شناخته می شود. این یک مایع سبک، بی رنگ با بویی ملایم و تا حدودی شیرین (مشابه بوی اتانول) است. به دلیل ساختار تک کربنه و وجود گروه هیدروکسیل، متانول دارای خواص شیمیایی منحصربفردی است که آن را هم مفید و هم خطرناک می کند. این ترکیب به شدت قابل اشتعال است و با شعله ای تقریباً نامرئی می سوزد و دی اکسید کربن و آب تولید می کند. متانول به طور کامل با آب و بسیاری از حلال های آلی مخلوط می شود که این نشان دهنده ی قطبیت آن است. ترکیبی از فراریت، قطبیت و واکنش پذیری متانول پایه بسیاری از کاربردهای صنعتی آن است از کاربرد به عنوان حلال و ضد یخ گرفته تا استفاده به عنوان سوخت و ماده اولیه در سنتز های شیمیایی. به همین دلیل، خرید حواله متانول برای واحدهای تولیدی و بازرگانان مواد شیمیایی از اهمیت ویژه ای برخوردار است. در بخش های بعدی خواص شیمیایی متانول را با جزئیات بررسی می کنیم و ساختار، واکنش ها و ملاحظات ایمنی مربوط به آن را پوشش می دهیم.
ساختار شیمیایی و ترکیب متانول
متانول از یک اتم کربن تشکیل شده که به سه اتم هیدروژن و یک گروه هیدروکسیل (-OH) متصل است. این ساختار مولکولی (CH3OH) آن را به ساده ترین عضو خانواده الکل ها تبدیل می کند. اتم کربن بخشی از یک گروه متیل (CH3–) است که به اکسیژن گروه هیدروکسیل پیوند یافته و پیوندی کووالانسی قطبی را تشکیل داده است. پیوند O–H در مولکول مسئول بسیاری از خواص شیمیایی متانول است، از جمله توانایی آن در تشکیل پیوند هیدروژنی. متانول خالص اغلب الکل متیلیک یا الکل چوب نامیده می شود. نام الکل چوب به دلیل تولید تاریخی آن از تقطیر مخرب چوب بر روی این ماده گذاشته شده است. جرم مولی این مولکول حدود ۳۲٫۰۴ گرم بر مول است و در دمای اتاق به صورت مایع بی رنگ ظاهر می شود. اندازه کوچک و حضور گروه قطبی -OH به متانول درجه بالایی از واکنش پذیری شیمیایی داده است، با وجود اینکه مولکولی بسیار ساده است. گروه هیدروکسیل محل وقوع واکنش های نوع الکل است و به متانول اجازه می دهد علی رغم ساختار ساده خود در انواع واکنش های شیمیایی شرکت کند. به طور کلی ساختار متانول به عنوان یک الکل تک کربنه زیربنای رفتار فیزیکی و شیمیایی آن است.
ویژگی های فیزیکی و ظاهر
در حالت خالص، متانول یک مایع شفاف و بی رنگ است که از نظر روانی شبیه به آب می باشد. این مایع بویی خفیف و تا حدودی شیرین شبیه اتانول دارد، هرچند متانول قابل نوشیدن نیست و بسیار سمی است. ویژگی های فیزیکی متانول بازتاب دهنده اندازه کوچک و ماهیت قطبی آن هستند و بسیاری از خواص فیزیکی متانول مانند نقطه جوش پایین، چگالی کم و قابلیت امتزاج بالا را تعیین می کنند. نقطه جوش آن حدود ۶۴٫۷ °C است که نسبتاً پایین می باشد و نشان می دهد متانول در دمای اتاق به سرعت تبخیر می شود (فراریت بالایی دارد). نقطه انجماد آن ۹۷٫۶- °C است، به این معنی که تا دماهای بسیار پایین نیز به صورت مایع باقی می ماند. چگالی متانول در دمای ۲۰ °C حدود ۰٫۷۹ گرم بر سانتی متر مکعب است که کمتر از چگالی آب می باشد. متانول به راحتی با آب مخلوط می شود و با بسیاری از حلال های آلی نیز قابل امتزاج است و محلول های یکنواخت تشکیل می دهد. بخار متانول کمی سنگین تر از هوا است و می تواند در نقاط پایین تجمع پیدا کند. هنگام سوختن، متانول شعله ای آبی کم رنگ تولید می کند که تقریباً نامرئی است. به طور کلی، ظاهر فیزیکی و رفتار متانول بی رنگ، فرار و قابل اشتعال مشخصه یک الکل سبک است و با ساختار مولکولی و پیوندهای آن همخوانی دارد.
قطبیت و تشکیل پیوند هیدروژنی
متانول یک مولکول قطبی است به دلیل حضور گروه -OH هیدروکسیل و اتم اکسیژن الکترونگاتیو در آن. اکسیژن چگالی الکترونی را از کربن و هیدروژن به سمت خود می کشد و در مولکول یک گشتاور دوقطبی دائمی ایجاد می کند. گشتاور دوقطبی متانول حدود ۱٫۷ دبی است که نشانگر قطبیت قابل توجهی برای چنین مولکول کوچکی است. یکی از نتایج این قطبش، توانایی متانول در تشکیل پیوند هیدروژنی است. هر مولکول متانول می تواند با مولکول های دیگر یا با مولکول های آب پیوند هیدروژنی برقرار کند (به عنوان دهنده ضعیف پیوند هیدروژنی و نیز پذیرنده آن). این تعاملات پیوند هیدروژنی باعث شده متانول نقطه جوش بالاتری نسبت به مولکول های غیرقطبی با وزن مولکولی مشابه داشته باشد. مثلاً متان (CH4) جرم مولی نزدیکی دارد اما در دمای اتاق گاز است، در حالی که متانول به دلیل اینکه مولکول های آن از طریق پیوند هیدروژنی یکدیگر را جذب می کنند، مایع است. نیروهای بین مولکولی قوی همچنین به حلالیت عالی متانول در حلال های قطبی کمک می کنند. به طور خلاصه، ماهیت قطبی متانول و ظرفیت آن در پیوند هیدروژنی از خواص شیمیایی کلیدی این ماده است که بر رفتار حلالیت، نقطه جوش و امتزاج پذیری آن با آب تأثیر می گذارد.
حلالیت و امتزاج پذیری
یکی از ویژگی های قابل توجه متانول، امتزاج پذیری کامل آن با آب است. متانول می تواند با آب در هر نسبتی مخلوط شود و یک فاز همگن ایجاد کند. این به دلیل توانایی متانول در تشکیل پیوند هیدروژنی با آب و ماهیت قطبی آن است که به آن اجازه می دهد با مولکول های آب تعامل مطلوبی داشته باشد. در واقع، متانول اغلب برای حل کردن موادی به کار می رود که آب به تنهایی قادر به حل کردن آن ها نیست و به عنوان یک حلال کمکی در مخلوط های آبی عمل می کند. علاوه بر آب، متانول با بسیاری از حلال های آلی نیز قابل امتزاج است، مانند اتانول، اتر دی اتیل و استون. متانول تا حدی دنیای قطبی و غیرقطبی را به هم پیوند می دهد در حالی که یک حلال پروتیک قطبی است، گروه هیدروکربنی کوچک (متیل) آن کمی سازگاری با ترکیبات آلی به آن می بخشد. هر چه زنجیر کربنی الکل ها بلندتر شود (اتانول، پروپانول و غیره)، حلالیت آن ها در آب کاهش می یابد، اما متانول به عنوان کوتاه ترین الکل کاملاً در آب حل می شود. به خاطر این ویژگی حلالیت، متانول به عنوان یک حلال صنعتی برای رزین ها، مرکب ها و چسب ها استفاده می شود. متانول می تواند طیف گسترده ای از مواد شیمیایی را حل کند که این منعکس کننده دوگانگی آب دوست-آب گریز مولکول آن است. این امتزاج پذیری استثنایی یکی از دلایل اصلی کاربرد متانول به عنوان حلال در آزمایشگاه ها و صنعت می باشد.
قابلیت اشتعال و خواص احتراق
متانول به شدت قابل اشتعال است و ویژگی های آن در ارتباط با آتش نیازمند توجه دقیق می باشد. نقطه اشتعال متانول حدود ۱۱ °C است، یعنی در دماهایی کمی بالاتر از دمای اتاق می تواند بخار کافی برای احتراق در هوا تولید کند. بخارات متانول در محدوده وسیعی از غلظت ها با هوا مخلوط انفجاری تشکیل می دهند (حدود ۶٪ تا ۳۶٪ متانول حجمی در هوا). پس از اشتعال، متانول به سرعت می سوزد و دی اکسید کربن و آب را به عنوان محصولات احتراق تولید می کند H2O ۲ CH3OH + ۳ O2 → ۲ CO2 + ۴ . قابل ذکر است که شعله متانول تقریباً بی رنگ و آبی کم رنگ است و در نور روز تقریباً ناپیدا می باشد؛ این یک خطر ایمنی جدی است، زیرا ممکن است آتش متانول حتی در حضور گرمای شدید فوراً دیده نشود. احتراق متانول نسبت به هر واحد حجم انرژی کمتری نسبت به بنزین آزاد می کند (محتوای انرژی آن پایین تر است)، اما پاک تر می سوزد و دوده بسیار کمی تولید می کند. عدد اکتان بالای متانول و احتراق تمیز آن باعث شده که به عنوان سوخت در موتورهای با کارایی بالا و مسابقه ای مطرح باشد. در مجموع، قابلیت اشتعال متانول هم استفاده مهم آن را به عنوان سوخت ممکن می سازد و هم یک ریسک بزرگ در هنگام کار با آن محسوب می شود.
سمیت و اثرات بر سلامتی
متانول برای انسان ها و بسیاری از جانوران بسیار سمی است. بر خلاف اتانول که نسبتاً بدون خطر متابولیزه می شود، متانول توسط کبد به فرمالدهید و سپس اسید فرمیک تبدیل می شود – هر دوی این متابولیت ها سمی هستند. حتی مقدار کمی متانول (حدود ۱۰ تا ۱۵ میلی لیتر متانول خالص) می تواند اثرات جدی بر سلامتی داشته باشد، از جمله کوری دائمی به دلیل آسیب به عصب بینایی. مقداری کمی بزرگتر (حدود ۲۰ تا ۳۰ میلی لیتر) در صورت عدم درمان ممکن است کشنده باشد. علائم مسمومیت با متانول (سردرد، سرگیجه, تهوع، تاری دید) معمولاً با تأخیر ظاهر می شوند و چند ساعت پس از مواجهه شدید می شوند، زیرا متابولیت های سمی به تدریج انباشته می شوند. متانول نه تنها از طریق نوشیدن بلکه با استنشاق بخارات یا جذب پوستی نیز وارد بدن می شود، اگرچه بلعیدن شایع ترین مسیر خطرناک است. به خاطر سمیت آن، متانول به عنوان یک ماده افزودنی تلخ کننده برای اتانول صنعتی استفاده می شود آن را عمداً اضافه می کنند تا اتانول غیرقابل نوشیدن شود. هیچ طعم یا بوی قابل اعتمادی وجود ندارد که حضور متانول را در یک نوشیدنی نشان دهد و همین امر به موارد مسمومیت تصادفی یا عمدی انجامیده است. خلاصه اینکه تبدیل متابولیک متانول به اسید فرمیک علت خطرناک بودن آن است و موجب اسیدوز متابولیک و آسیب به بافت ها می شود.
رفتار اسیدی و بازی متانول
از نظر شیمیایی، متانول یک اسید بسیار ضعیف و یک باز بسیار ضعیف است. به عنوان یک اسید، می تواند پروتون گروه هیدروکسیل خود را اهدا کند، اما این تنها در حضور بازهای قوی اتفاق می افتد. ثابت تفکیک اسیدی (pKa) متانول حدود ۱۵٫۵ است که تقریباً با آب (۱۵٫۷) برابر است و نشان می دهد که بسیار ضعیف تر از اسیدهای قوی مانند اسید استیک (حدود ۴٫۸) می باشد. این یعنی در محلول آبی، متانول تقریباً به طور کامل به صورت مولکول CH3OH باقی می ماند و تشکیل یون متوکسید (CH3O–) ناچیز است. اما اگر متانول در معرض یک فلز واکنش پذیر یا باز قوی قرار گیرد، پروتون خود را از دست می دهد؛ مثلاً فلز سدیم با متانول واکنش داده و متوکسید سدیم (CH3ONa) و گاز هیدروژن تولید می کند. این واکنش مشابه واکنش سدیم با آب است اما کندتر و کم شدت تر، زیرا اسیدیته متانول پایین تر است. برعکس، متانول می تواند به عنوان یک باز بسیار ضعیف عمل کند و در شرایط کاملاً اسیدی (مثلاً در تماس با اسید معدنی قوی) پروتون اضافی جذب کرده و یون متیل اکسونیم (CH3OH2+) را تشکیل دهد. این گونه یون دار ناپایدار معمولاً به عنوان گونه واسطه در واکنش های کاتالیز شده با اسید ظاهر می شود. خلاصه اینکه در شرایط عادی متانول تقریباً خنثی است، اما در حضور واکنشگرهای بسیار قوی می تواند با دادن یا گرفتن پروتون در شیمی اسید-باز شرکت کند.
واکنش های اکسیداسیون و محصولات جانبی
متانول مستعد واکنش های اکسیداسیون است، با توجه به اینکه کربن آن در حالت اکایش نسبتاً پایینی (-۲) قرار دارد. وقتی متانول تحت شرایط اکسنده قرار گیرد، می تواند به ترتیب به محصولات اکسید شده تری تبدیل شود. محصول اولیه اکسیداسیون، فرمالدهید (CH2O) است. مثلاً با یک کاتالیزور (مانند سیمان نقره داغ یا مس) و حضور اکسیژن، بخار متانول می تواند دهیدروژنه شده و به فرمالدهید تبدیل شود و آب نیز به عنوان محصول جانبی تولید گردد. این واکنش مبنای تولید صنعتی فرمالدهید از متانول است. اگر اکسیداسیون بیشتر ادامه یابد (یا اگر اکسنده قوی تر حضور داشته باشد)، فرمالدهید می تواند به اسید فرمیک (HCOOH) اکسید شود. در شرایط شدیدتر یا در صورت احتراق کامل، کربن متانول سرانجام به دی اکسید کربن (CO2) تبدیل می شود. در آزمایشگاه، اکسنده های کلاسیک مانند پرمنگنات پتاسیم یا دی کرومات نیز متانول را ابتدا به فرمالدهید و سپس در صورت اضافی بودن عامل اکسنده به اسید فرمیک یا CO2 اکسید می کنند. این مسیرهای اکسیداسیون پیامدهای عملی دارند: اثرات سمی متانول در بدن ناشی از اکسایش متابولیک آن به اسید فرمیک است، و در صنعت نیز اکسیداسیون کنترل شده متانول مواد شیمیایی مهمی مانند فرمالدهید را فراهم می کند. بنابراین، سهولت اکسیداسیون متانول یک خاصیت شیمیایی اساسی است که می تواند هم مفید و هم مضر باشد.
تشکیل استر و اتر
متانول به راحتی در واکنش های استری سازی شرکت می کند و تحت شرایط مناسب اترها را نیز تشکیل می دهد. به عنوان یک الکل کوچک، متانول با اسیدهای کربوکسیلیک واکنش می دهد و استرهای متیل تولید می کند. مثلاً واکنش متانول با اسید استیک، متیل استات (CH3COOCH3) و آب تولید می کند، به ویژه در حضور کاتالیزور اسیدی. این نوع واکنش – ترکیب یک الکل و یک اسید به طور گسترده استفاده می شود؛ یکی از کاربردهای مهم آن تولید بیودیزل است که در آن متانول اسیدهای چرب (از روغن ها) را به استرهای متیل اسید چرب تبدیل می کند. در حضور اسیدهای قوی یا عوامل آب زدا، دو مولکول متانول می توانند با هم ترکیب شوند و یک اتر ایجاد کنند. به طور صنعتی، متانول را روی آلومینا یا کاتالیزور مشابه، آبگیری می کنند تا دی متیل اتر (CH3OCH3) تولید شود که یک پیشران مهم در افشانه ها و سوخت بالقوه محسوب می شود. متانول حتی می تواند به آلکن ها افزوده شود؛ مثلاً با ایزوبوتن ترکیب شده و متیل ترت-بوتیل اتر (MTBE) تولید می کند که به عنوان افزودنی بنزین به کار رفته است. این واکنش ها نشان می دهند متانول چقدر در تشکیل مشتقات متنوع انعطاف پذیر است، به طوری که می تواند هیدروژن گروه هیدروکسیل خود را جایگزین کرده یا گروه متیل آن به گروه های عاملی دیگر متصل شود.
تبدیلات صنعتی و مشتقات متانول
خواص شیمیایی متانول باعث شده این ماده به ماده اولیه کلیدی در صنایع شیمیایی تبدیل شود. بخش بزرگی از متانول جهان از طریق فرآیندهای صنعتی به دیگر مواد شیمیایی تبدیل می شود. یکی از تبدیل های اصلی، تولید فرمالدهید است (همان طور که پیشتر ذکر شد): متانول در حضور کاتالیزور اکسید می شود و فرمالدهید حاصل می گردد که برای ساخت رزین ها، پلاستیک ها و چسب ها استفاده می شود. فرآیند مهم دیگر، تولید اسید استیک از طریق کربونیلاسیون متانول (فرآیندهای مونسانتو و کاتیوا) است در این فرآیند متانول با مونوکسید کربن (به کمک کاتالیزور) واکنش داده و اسید استیک را در مقیاس بزرگ تولید می کند. متانول همچنین برای تولید متیل ترشیو بوتیل اتر (MTBE) از طریق واکنش با ایزوبوتن استفاده می شود؛ MTBE به عنوان تقویت کننده عدد اکتان بنزین به کار رفته است. افزون بر این، متانول را می توان آبگیری کرد و به الفین ها و هیدروکربن های بنزین دار تبدیل نمود در فرآیندهایی مانند MTO یعنی تبدیل متانول به الفین و MTG یعنی تبدیل متانول به بنزین، که نشان می دهد متانول می تواند به عنوان یک ماده سازنده برای سوخت ها عمل کند. تولید متیل آمین ها (از واکنش متانول با آمونیاک روی کاتالیزور) نیز مسیر صنعتی مهم دیگری است که ترکیباتی برای صنایع دارویی و کشاورزی فراهم می کند. در مجموع انعطاف پذیری متانول در تبدیل به گستره وسیعی از مواد شیمیایی از حلال ها و سوخت ها گرفته تا پلیمرها نقش مرکزی آن را در صنایع شیمیایی نمایان می سازد.
متانول به عنوان سوخت
استفاده از متانول به عنوان سوخت ناشی از ویژگی های احتراقی و عدد اکتان بالای آن است. متانول را می توان در موتورهای احتراق داخلی یا به صورت خالص یا به عنوان افزودنی به بنزین به کار برد. در واقع، متانول در مسابقات با کارایی بالا مثلاً سابقاً در IndyCar به عنوان سوخت استفاده شده است، زیرا خنک تر از بنزین می سوزد و می تواند توان خروجی بالایی تولید کند. عدد اکتان بالای متانول یعنی متانول می تواند بدون احتراق خودبه خودی در برابر تراکم مقاومت کند که برای عملکرد موتور مفید است. در هنگام سوختن، متانول دی اکسید کربن و آب تولید می کند و دود یا دوده بسیار کمی دارد، بنابراین گاز خروجی آن نسبت به بنزین یا دیزل تمیزتر است. با این حال، محتوای انرژی متانول در هر لیتر تقریباً نصف بنزین است، بنابراین یک خودرو نیاز به سوخت گیری مکررتر یا مخزن بزرگ تر دارد تا مسافت مشابهی را طی کند. متانول همچنین این مزیت را دارد که به صورت مایع در دمای محیط است (بر خلاف هیدروژن یا گاز طبیعی که گازی هستند)، که ذخیره و جابجایی آن را به عنوان یک سوخت جایگزین آسان تر می کند. ایده اقتصاد متانول هنوز مورد توجه است؛ مفهومی که در آن متانول به عنوان یک سوخت مایع تجدیدپذیر و حامل انرژی به کار می رود (برای مثال متانول را می توان از زیست توده یا ترکیب دی اکسید کربن و هیدروژن تولید کرد و چرخه سوخت کربن خنثی ایجاد کرد).
متانول به عنوان حلال در صنعت
خواص حلال بودن متانول باعث شده است که در کاربردهای مختلف صنعتی و آزمایشگاهی بسیار مفید باشد. چون متانول یک حلال قطبی پروتیک است (قادر به ایجاد پیوند هیدروژنی)، می تواند بسیاری از مواد از جمله نمک ها، ترکیبات آلی و حتی برخی گازها را بهتر از حلال های غیرقطبی حل کند. متانول به عنوان حلال در تولید داروها استفاده می شود، جایی که می تواند برای استخراج یا تبلور مجدد ترکیبات به کار رود. همچنین یک حلال متداول برای رنگ ها، جوهرها و رنگدانه ها است و به تنظیم ویسکوزیته و زمان خشک شدن کمک می کند. در صنعت نفت، متانول را به خطوط لوله تزریق می کنند تا از تشکیل هیدرات ها (ترکیبات یخ مانند) جلوگیری شود، زیرا با حل کردن آب و پایین آوردن نقطه انجماد آن عمل می کند، در واقع نقش ضد یخ را دارد. در گذشته، متانول به عنوان ضدیخ خودرو و مایع شیشه شوی نیز استفاده می شد، زیرا نقطه انجماد آب را به شکل مؤثری کاهش می دهد؛ اما از سال های اخیر به دلیل سمیت آن استفاده از متانول در محصولات مصرفی مانند شیشه شوی ها در بعضی مناطق ممنوع یا محدود شده است. متانول همچنین به عنوان پاک کننده و حتی به عنوان ماده واکنش دهنده در برخی واکنش های شیمیایی به کار می رود که در آن نقش حلال و واکنشگر را به طور همزمان ایفا می کند. نقطه جوش پایین متانول اجازه می دهد پس از اتمام کار به راحتی با تبخیر از محلول جدا شود. در مجموع، چندکاره بودن متانول به عنوان حلال نتیجه ترکیب قطبیت، توانایی پیوند هیدروژنی و فراریت آن است.
مقایسه با اتانول و سایر الکل ها
در مقایسه با سایر الکل های رایج، متانول علی رغم تعلق به همان خانواده تفاوت های آشکاری در خواص شیمیایی دارد. اتانول (C2H5OH)، پروپانول (C3H7OH) و بوتانول (C4H9OH) به ترتیب زنجیر کربنی بزرگ تری دارند. با افزایش طول زنجیر، مولکول ها به طور کلی قطبیت کمتری پیدا می کنند و خواص فیزیکی آن ها تغییر می کند. متانول پایین ترین نقطه جوش را در این سری دارد ۶۴٫۷ °C ، در حالی که اتانول در ۷۸٫۴ °C می جوشد و ۱-بوتانول در حدود ۱۱۷ °C. این روند به دلیل افزایش وزن مولکولی و اندکی کاهش توان نسبی پیوند هیدروژنی است الکل های بزرگ تر نیروهای پراکندگی بیشتری دارند اما گروه OH درصد کوچکتری از مولکول را تشکیل می دهد. متانول و اتانول به طور کامل در آب قابل امتزاج هستند، در حالی که ۱-بوتانول تنها به صورت محدود محلول است؛ این موضوع نشان می دهد که زنجیر کربنی آب گریز در الکل های بزرگ تر مانع از اختلاط کامل با آب می شود. از نظر سمیت نیز متانول متفاوت است: اتانول به اندازه ای ایمن است که به صورت نوشیدنی مصرف شود (در حد اعتدال)، اما حتی مقدار کمی متانول می تواند مسمومیت شدید ایجاد کند. مولکول کوچک تر متانول فرّارتر است و در دماهای پایین تری مشتعل می شود نسبت به الکل های سنگین تر نقطه اشتعال آن پایین تر از اتانول است، و نقطه اشتعال ۱-بوتانول بسیار بالاتر، حدود ۲۹ °C. جدول زیر برخی تفاوت های کلیدی بین متانول و چند الکل دیگر را خلاصه می کند:
| مشخصه | متانول (CH3OH) | اتانول (C2H5OH) | ۱-پروپانول (C3H7OH) | ۱-بوتانول (C4H9OH) |
|---|---|---|---|---|
| وزن مولکولی (گرم بر مول) | ۳۲.۰۴ | ۴۶.۰۷ | ۶۰.۱۰ | ۷۴.۱۲ |
| نقطه جوش (درجه سانتی گراد) | ۶۴.۷ | ۷۸.۴ | حدود ۹۷ | حدود ۱۱۷ |
| نقطه ذوب (درجه سانتی گراد) | ۹۷.۶- | ۱۱۴.۵- | ۱۲۶- | ۹۰- |
| چگالی (g/cm³ در ۲۰ درجه) | ۰.۷۹ | ۰.۷۹ | ۰.۸۰ | ۰.۸۱ |
| حلالیت در آب | کاملا قابل امتزاج | کاملا قابل امتزاج | کاملا قابل امتزاج | حدود ۸ گرم در ۱۰۰ میلی لیتر (۲۰ درجه) |
| نقطه اشتعال (درجه سانتی گراد) | ۱۱ | ۱۳ | ۱۵ | ۲۹ |
| سمیت (مصرف خوراکی) | بسیار بالا (کوری یا مرگ) | متوسط (مستی) | متوسط (غیر خوراکی) | متوسط (محرک) |





بررسی قطبیت و حلالیت متانول در آب و حلال های آلی و کاربردهای صنعتی و آزمایشگاهی آن
بررسی واکنش های اکسیداسیون متانول و کاربردهای صنعتی آن
بررسی مکانیزم واکنش های استری سازی متانول و نقش کاتالیزورها
آشنایی با سایر واکنش های شیمیایی متانول (مانند تشکیل هیدروژن از متانول) و نقش آن ها در فرآیندهای صنعتی و انرژی محور