فهرست عناوین
- مقدمه
- خواص متانول مرتبط با اکسیداسیون
- مسیرهای متداول اکسیداسیون متانول
- احتراق کامل متانول به عنوان سوخت
- اکسیداسیون جزئی متانول به فرمالدهید
- اکسیداسیون متانول به اسید فرمیک و CO₂
- عوامل اکسنده شیمیایی برای متانول
- اکسیداسیون الکتروشیمیایی در پیل های سوختی
- اکسیداسیون زیستی و سوخت و ساز متانول
- اکسیداسیون متانول برای تولید هیدروژن
- مقایسه فرایندهای عمده اکسیداسیون متانول
- سازوکار واکنش در اکسیداسیون متانول
- کاربردهای صنعتی اکسیداسیون متانول
نوشته شده توسط شرکت صنایع متانول ایران
منتشر شده توسط شرکت صنایع متانول ایران
تاریخ انتشار مقاله : 02-10-1404
تاریخ بروزرسانی مقاله : 02-10-1404
تعداد کلمات : 3300
آدرس مقاله : لینک مقاله
واکنش های اکسیداسیون متانول

مقدمه
متانول (CH₃OH) که به عنوان الکل متیلیک یا الکل چوب نیز شناخته می شود، ساده ترین الکل است و یک ماده اولیه شیمیایی و سوخت پرکاربرد است. واکنش های اکسیداسیون متانول یک جنبه اساسی هم در شیمی آلی و هم در علم انرژی محسوب می شوند. در این واکنش ها، متانول از طریق افزودن اکسیژن یا حذف هیدروژن به صورت شیمیایی تغییر یافته و محصولات متنوعی مانند فرمالدهید، اسید فرمیک، دی اکسید کربن و آب تولید می کند. درک نحوه اکسید شدن متانول حائز اهمیت است زیرا این الکل تک کربنه ساده می تواند به عنوان یک سوخت پاک سوزانده شود، به مواد شیمیایی مهم تبدیل گردد و حتی توسط موجودات زنده متابولیزه شود؛ موضوعی که امروزه نه تنها در مباحث علمی بلکه در تصمیم های تجاری و زنجیره تامین مانند خرید حواله متانول زاگرس نیز اهمیت عملی پیدا کرده است. بخش های زیر دیدگاهی جامع از مسیرهای اکسیداسیون متانول ارائه می دهند؛ از احتراق کامل گرفته تا اکسیداسیون های جزئی و فرایندهای کاتالیزی، با تأکید بر کاربردهای عملی و شیمی پایه ای هر کدام.
خواص متانول مرتبط با اکسیداسیون
متانول یک مایع سبک، فرار و اشتعال پذیر با فرمول شیمیایی CH₃OH است. از آنجا که تنها یک اتم کربن دارد و یک الکل نوع اول است، در شرایط مختلف به راحتی اکسید می شود. ساختار مولکولی آن یک گروه متیل متصل به یک گروه هیدروکسیل موجب می گردد که برای اکسیداسیون نیازی به شکست پیوند کربن–کربن نباشد. متانول نقطه جوش پایینی دارند ~۶۵ °C و نقطه اشتعال آن حدود ۱۱ °C است که نشان می دهد به سادگی بخارات قابل اشتعال تولید می کند. در هنگام احتراق، متانول با شعله آبی کم رنگی می سوزد که در روشنایی روز تقریباً نامرئی به نظر می رسد. این ویژگی ها نشان می دهند که متانول به چه سهولتی واکنش های اکسیداسیون با اکسیژن هوا انجام داده و انرژی را به صورت گرما آزاد می کند. اندازه کوچک متانول و محتوای اکسیژن بالای آن باعث می شود که ذاتاً سوختی با احتراق پاک باشد و دوده کربنی تولید نکند. از نظر شیمیایی، متانول می تواند توسط گستره ای از عوامل اکسید کننده اکسید شود که نشان دهنده واکنش پذیری آن به عنوان ساده ترین الکل است. ترکیب اشتعال پذیری بالا و واکنش پذیری، رفتار متانول در فرایندهای اکسیداسیون در صنایع و محیط طبیعی را تعیین می کند.
مسیرهای متداول اکسیداسیون متانول
مسیرهای اکسیداسیون متانول معمولاً به صورت مرحله به مرحله پیش می رود و طی آن حالت اکسایش کربن به تدریج افزایش می یابد. به عنوان یک الکل نوع اول، متانول ابتدا می تواند به یک آلدهید فرمالدهید، CH₂O اکسید شود، سپس به یک اسید کربوکسیلیک اسید فرمیک، HCOOH و در نهایت در صورت اکسایش کامل به دی اکسید کربن (CO₂) تبدیل گردد. از نظر شیمی اکسیداسیون، کربن متانول در آغاز دارای حالت اکسایش نسبتاً پایینی (–2) است و در CO₂ به +4 می رسد. هر گام اکسایش شامل افزوده شدن اکسیژن یا از دست دادن هیدروژن از مولکول متانول است. برای مثال، اکسایش اولیه دو اتم هیدروژن را از متانول جدا می کند تا فرمالدهید تشکیل شود (CH₃OH → CH₂O + H₂) . افزودن بیشتر اکسیژن به فرمالدهید اسید فرمیک (CH₂O + O → HCOOH) ایجاد می کند و اکسایش بعدی دی اکسید کربن آزاد می کند (HCOOH → CO₂ + H₂) . این مسیرهای اکسیداسیون می توانند تحت شرایط مختلف رخ دهند: عوامل اکسید کننده ضعیف تر واکنش را در حد تشکیل فرمالدهید متوقف می کنند، در حالی که اکسید کننده های قوی یا ادامه واکنش، اکسایش را تا CO₂ پیش می برند. درک این مسیرها مهم است زیرا نحوه تبدیل متانول را هم در واکنش های کنترل شده شیمیایی و هم در حالات خارج از کنترل مثل آتش سوزی ها نشان می دهد.
احتراق کامل متانول به عنوان سوخت
متانول در حضور اکسیژن به راحتی می سوزد و گرمای قابل توجهی آزاد می کند. واکنش احتراق کامل متانول را می توان با معادله موازنه شده زیر نمایش داد: 2 CH₃OH + 3 O₂ → 2 CO₂ + 4 H₂O . در موتورهای احتراقی یا شعله، بخار متانول با هوا مخلوط شده و مشتعل می شود و در نتیجه محصولات نهایی اکسیداسیون یعنی دی اکسید کربن و بخار آب تولید می گردد. احتراق متانول در مقایسه با هیدروکربن های سنگین تر تمیز است نه دوده جامد و نه اکسیدهای گوگرد تولید نمی کند و ذرات معلق بسیار کمتری آزاد می کند. دمای شعله متانول از بنزین پایین تر است که می تواند منجر به تشکیل کمتر اکسیدهای نیتروژن (NOx) شود. با این حال، احتراق ناقص یا شرایط روشن کردن سرد ممکن است مقداری مونوکسید کربن یا فرمالدهید به عنوان محصولات اکسیداسیون جزئی ایجاد کند. عدد اکتان متانول بالا است (بیش از 100)، به این معنی که می تواند سوخت موتورهای با تراکم بالا را به طور کارآمد تأمین کند. البته چگالی انرژی متانول کمتر از بنزین است (حدود نصف انرژی در هر لیتر)، بنابراین برای همان خروجی انرژی حجم سوخت بیشتری نیاز است. با این وجود، خاصیت پاک سوزی متانول و امکان تولید آن از منابع تجدیدپذیر، این سوخت را در برخی کاربردها از خودروهای مسابقه گرفته تا مولدهای برق جذاب کرده است.
اکسیداسیون جزئی متانول به فرمالدهید
اکسیداسیون جزئی کنترل شده متانول منجر به تولید فرمالدهید (CH₂O) می شود که یک ماده شیمیایی صنعتی بسیار پرکاربرد است. تولید فرمالدهید از متانول معمولاً با عبور مخلوط بخار متانول و هوا از روی یک کاتالیزگر در دمای بالا انجام می گیرد. در گذشته، از کاتالیزگر نقره در حدود 600 ° Cاستفاده می شد تا فرمالدهید و آب از متانول تولید شود: 2 CH₃OH + O₂ → 2 CH₂O + 2 H₂O . در کارخانه های مدرن اغلب از کاتالیزگر اکسید آهن-مولیبدن در ~300 ° Cپفرآیند Formox برای رسیدن به بازده بالا استفاده می کنند. در هر دو حالت، متانول دهیدروژنه شده و به فرمالدهید اکسید می شود و سپس سرد شده و در آب جذب می گردد تا محلول ۳۷٪ فرمالین به دست آید یا برای مراحل بعدی فرآوری می شود. این واکنش گرماده است و باید با دقت کنترل شود تا از اکسید شدن بیش از حد فرمالدهید به اسید فرمیک یا CO₂ جلوگیری گردد. فرمالدهید یکی از مواد شیمیایی با حجم تولید بسیار بالا از متانول است: حدود یک سوم مصرف متانول جهان به تبدیل آن به فرمالدهید اختصاص می یابد که در ساخت رزین ها، پلاستیک ها و سایر محصولات به کار می رود. اکسیداسیون جزئی متانول به فرمالدهید به این ترتیب یکی از پایه های صنعت شیمیایی متانول است.
اکسیداسیون متانول به اسید فرمیک و CO₂
وقتی متانول (یا حد واسط آن فرمالدهید) تحت شرایط اکسایش شدیدتری قرار گیرد، واکنش می تواند اسید فرمیک (HCOOH) را که یک اسید کربوکسیلیک تک کربنه است تولید کند. در شرایط آزمایشگاهی، اگر متانول با استفاده از مقادیر زیاد عوامل اکسنده قوی (مانند پرمنگنات پتاسیم داغ یا اسید کرومیک اضافی) اکسید شود، هر فرمالدهید واسطه ای که تشکیل گردد نیز به اسید فرمیک اکسید خواهد شد. تبدیل فرمالدهید به اسید فرمیک شامل افزودن یک اتم اکسیژن به گروه کربونیل است و عملاً یک اسید کربوکسیلیک تولید می کند. خود اسید فرمیک نیز می تواند بیشتر به دی اکسید کربن و آب اکسید شود، به ویژه در حضور اکسید کننده های بسیار قوی یا شرایط کاتالیزی در دمای بالا. از آنجا که متانول هیچ پیوند کربن–کربن ندارد، اکسید شدن کامل آن به CO₂ امکان پذیر است (و در واقع در احتراق و فرآیندهای سوخت و ساز رخ می دهد). در واکنش های کنترل شده، می توان با انتخاب شرایط مناسب، اسید فرمیک را جداگانه به دست آورد و واکنش را در مرحله تولید اسید متوقف کرد. اگرچه این مسیر یک راه صنعتی عمده نیست (معمولاً اسید فرمیک با روش های دیگری تولید می شود)، تشکیل اسید فرمیک از اکسیداسیون متانول از دیدگاه شناخت طیف کامل اکسیداسیون متانول قابل توجه است. شایان ذکر است که تجمع اسید فرمیک همچنین عامل اثرات مسمومیت با متانول در انسان است.
عوامل اکسنده شیمیایی برای متانول
در آزمایشگاه، متانول می تواند توسط انواع عوامل اکسنده شیمیایی اکسید شود. یک معرف کلاسیک، اسید کرومیک یا دی کرومات پتاسیم (K₂Cr₂O₇) در حضور اسید سولفوریک است که متانول را به فرمالدهید اکسید می کند؛ نشانه آن تغییر رنگ معرف از نارنجی (کروم VI) به سبز (کروم III) است. اگر واکنش ادامه یابد (یا اکسید کننده اضافی باشد)، فرمالدهید حاصل بیشتر به اسید فرمیک اکسید خواهد شد. برای جدا کردن فرمالدهید، شیمی دان ها اغلب از دستگاه تقطیر استفاده می کنند تا آن را به محض تشکیل خارج کنند و از اکسایش بیش از حد جلوگیری نمایند. پرمنگنات پتاسیم (KMnO₄) نیز یک اکسید کننده قوی دیگر است که می تواند متانول را اکسید کند؛ در محلول اسیدی معمولاً اسید فرمیک تولید می کند (با بی رنگ شدن رنگ بنفش KMnO₄ به دلیل کاهش به Mn²⁺ . سایر عوامل مانند اسید نیتریک یا معرف فنتون H₂O₂ با آهن نیز می توانند متانول را به محصولات اکسایش یافته تر تبدیل کنند. بدون حضور کاتالیزگر یا دمای بالا، متانول با اکسیژن محیط به سرعت واکنش نمی دهد برای شروع اکسیداسیون نیاز به منبع جرقه یا سطح کاتالیزی است. با این حال، حساسیت متانول به عوامل اکسید کننده شیمیایی یکی از جنبه های بنیادی شیمی آن است که به آن امکان تبدیل به ترکیبات با درجه اکسایش بالاتر را در بسیاری از واکنش های آزمایشگاهی می دهد.
اکسیداسیون الکتروشیمیایی در پیل های سوختی
در پیل های سوختی مستقیم متانول (DMFC)، متانول به صورت الکتروشیمیایی اکسید می شود و برق تولید می کند. در آند یک DMFC، یک کاتالیزگر (معمولاً پلاتین-روتنیم) اکسیداسیون متانول را در حضور آب تسهیل می کند: CH₃OH + H₂O → CO₂ + 6 H⁺ + 6 e⁻ . این نیم واکنش پروتون ها و الکترون هایی آزاد می کند؛ الکترون ها به صورت جریان الکتریکی در مدار خارجی جاری می شوند و پروتون ها از میان غشاء به سمت کاتد مهاجرت می کنند، جایی که با اکسیژن و الکترون ها ترکیب شده و آب تشکیل می دهند. حاصل نهایی این است که متانول به CO₂ اکسید می شود و انرژی آن مستقیماً به صورت توان الکتریکی به جای گرما آزاد می گردد. واکنش اکسیداسیون متانول در آند نیازمند کاتالیزگرهای مؤثر است زیرا گونه های واسطه مانند CO می توانند روی پلاتین جذب شده و آن را مسموم کنند. افزودن روتنیم به حذف اکسایشی این واسطه های CO کمک کرده و سطح کاتالیزگر را فعال نگه می دارد. DMFC ها در دماهای نسبتاً پایین حدود ۶۰–۱۲۰ °C کار می کنند و به عنوان فناوری امیدبخشی برای منابع توان قابل حمل مطرح هستند، زیرا سوخت مایع متانول نسبت به گاز هیدروژن آسان تر ذخیره و جابجا می شود. هرچند چالش هایی مانند بازده و عبور متانول از غشاء همچنان وجود دارد، پیل های سوختی متانولی نمایانگر روشی منحصر به فرد برای بهره گیری از اکسیداسیون در جهت تولید انرژی پاک هستند.
اکسیداسیون زیستی و سوخت و ساز متانول
در موجودات زنده، متانول توسط مسیرهای آنزیمی ویژه اکسید می شود. در انسان، متانول ابتدا توسط آنزیم الکل دهیدروژناز (در کبد) به فرمالدهید تبدیل می گردد. فرمالدهید بسیار سمی است و به سرعت توسط آنزیم دیگری (فرمالدهید دهیدروژناز و سپس فرمات دهیدروژناز) به اسید فرمیک اکسید می شود. تجمع اسید فرمیک در جریان خون به اسیدوز متابولیک و آسیب عصب بینایی منجر می گردد و به همین دلیل مصرف متانول می تواند باعث کوری یا مرگ شود. در نهایت، اسید فرمیک به دی اکسید کربن و آب متابولیزه می شود و مسیر اکسیداسیون را کامل می کند. انسان توان محدودی در پاکسازی فرمات دارد، که متانول را حتی در دوزهای نسبتاً کوچک نیز به شدت خطرناک می سازد. در برخی باکتری ها و مخمرهای خاص (متیلوتروف ها)، متانول به عنوان منبع کربن و انرژی استفاده می شود. این ارگانیسم ها آنزیم هایی مانند متانول دهیدروژناز تولید می کنند که متانول را به فرمالدهید اکسید می کند؛ سپس یا فرمالدهید را در بیومس خود ادغام می کنند یا آن را برای کسب انرژی بیشتر به CO₂ اکسید می کنند. بنابراین چه در کبد انسان و چه در باکتری خاک، متانول از طریق اکسیداسیون پیاپی به فرمالدهید، اسید فرمیک و CO₂ تبدیل می شود که مراحل شیمیایی اکسایش را تحت کنترل زیستی تقلید می کند.
اکسیداسیون متانول برای تولید هیدروژن
متانول می تواند از طریق فرآیندهای ریفورمینگ که شامل اکسایش هستند به یک منبع مناسب گاز هیدروژن تبدیل شود. یک روش، اکسیداسیون جزئی است که در آن متانول با مقدار محدودی اکسیژن واکنش می دهد و هیدروژن و دی اکسید کربن تولید می کند: CH₃OH + ½ O₂ → CO₂ + 2 H₂ این واکنش گرماده است و اغلب با ریفورمینگ با بخار واکنش درون گیر: CH₃OH + H₂O → CO₂ + 3 H₂در یک راکتور واحد ترکیب می شود (ریفورمینگ خودگرمایشی) تا بدون نیازبه گرمای خارجی، هیدروژن به صورت کارآمد تولید گردد. استفاده از متانول به عنوان حامل هیدروژن دارای مزایایی است: ریفورمینگ متانول در دماهای نسبتاً پایین (~250–300°C) اتفاق می افتد و حمل و نقل متانول مایع آسان تر از هیدروژن فشرده است. وجود کاتالیزگرها (معمولاً پایه مس یا فلزات گران بها) برای دستیابی به تبدیل و گزینش پذیری بالای این فرآیندها ضروری است. هیدروژن به دست آمده می تواند به پیل های سوختی یا فرآیندهای صنعتی خوراک دهی شود و یک منبع انرژی پاک تر را فراهم کند. مبدل های متانول به هیدروژن (ریفورمرها) برای خودروهای پیل سوختی پیشنهاد شده اند که به وسیله آن ها خودرو می تواند متانول مایع حمل کرده و بر حسب نیاز، هیدروژن را برای پیل سوختی هیدروژنی تولید کند. به طور کلی، اکسید کردن متانول به هیدروژن با تولید CO₂ به عنوان محصول جانبی یک مسیر مهم در زمینه ذخیره و تأمین انرژی به شمار می رود.
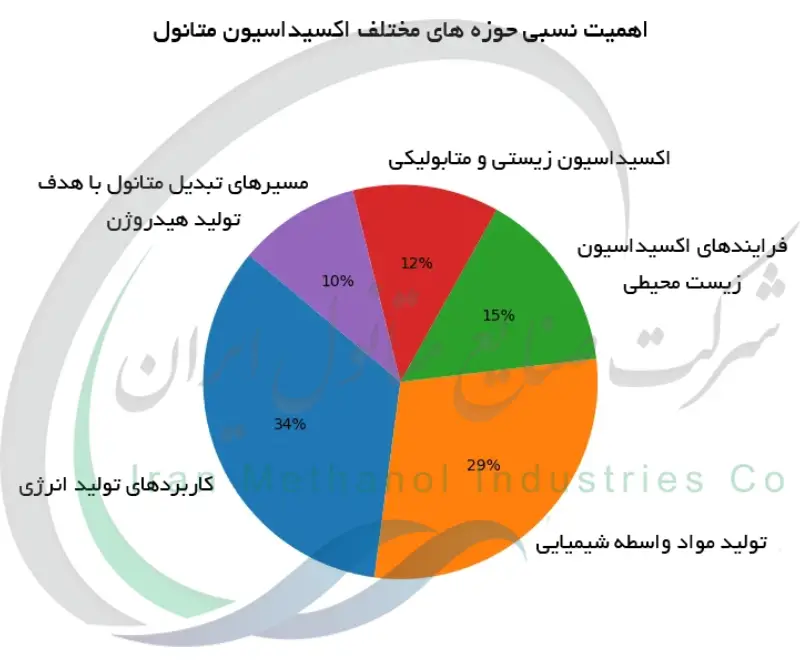
مقایسه فرایندهای عمده اکسیداسیون متانول
مسیرهای متعددی برای اکسیداسیون متانول وجود دارند که هر یک شرایط و محصولات متمایزی دارند. این مسیرها از سوزاندن متانول به عنوان سوخت گرفته تا اکسید کردن آن در واکنش های شیمیایی کنترل شده یا حتی درون سلول های زنده را شامل می شوند. جدول زیر چندین فرآیند کلیدی اکسیداسیون متانول را مقایسه می کند و واکنش، شرایط یا کاتالیزگرهای درگیر، محصولات اصلی و اهمیت آن ها را برجسته می سازد؛ مسیری که درک آن بدون توجه به قطبیت و حلالیت متانول در آب و حلال های آلی ناقص خواهد بود، زیرا این ویژگی ها نقش تعیین کننده ای در انتخاب محیط واکنش و نوع فرآیند اکسیداسیون دارند. برای مثال احتراق کامل در هوا تنها دی اکسید کربن و آب تولید می کند و آزادسازی انرژی را برای حرارت یا توان به حداکثر می رساند. یک اکسیداسیون کاتالیزی کنترل شده ممکن است در یک حد واسط مانند فرمالدهید متوقف شود که برای تولیدات شیمیایی مفید است. اکسیداسیون الکتروشیمیایی در یک پیل سوختی، برق را به طور مستقیم تولید می کند. اکسیداسیون زیستی در دمای محیط توسط آنزیم ها رخ می دهد و متانول را به متابولیت ها تبدیل می کند. هر فرآیند اهمیت خاص خود را دارد: برخی انرژی تولید می کنند، برخی مواد خام صنعتی به دست می دهند و برخی در چرخه های زیست محیطی یا فیزیولوژیک نقش دارند. با وجود تفاوت در محتوا، همه این ها شامل تغییر شیمیایی بنیادی متانول در واکنش با اکسیژن (یا اکسید کننده های معادل) به منظور تشکیل محصولات اکسید شده تر هستند. جدول زیر مروری پهلو به پهلو بر هشت مسیر اصلی اکسیداسیون متانول ارائه می دهد.
| فرایند اکسیداسیون | واکنش | شرایط / کاتالیزگر | محصولات اصلی | اهمیت |
|---|---|---|---|---|
| احتراق کامل | 2 CH₃OH + 3 O₂ → 2 CO₂ + 4 H₂O | شعله باز (حرارت، جرقه) | CO₂، H₂O (اکسایش کامل) | احتراق سوخت (بیشترین انرژی آزاد) |
| اکسیداسیون جزئی به فرمالدهید | 2 CH₃OH + O₂ → 2 CH₂O + 2 H₂O | کاتالیزگر نقره یا Fe-Mo (300–600°C) | CH₂O (فرمالدهید)، H₂O | تولید صنعتی فرمالدهید |
| اکسیداسیون به اسید فرمیک | CH₃OH + O₂ → HCOOH + H₂O | اکسید کننده قوی (مثلاً KMnO₄ در اسید) | HCOOH (اسید فرمیک)، H₂O | اکسایش در آزمایشگاه؛ اسید فرمیک (متابولیت سمی) |
| پیل سوختی مستقیم متانول (DMFC) | CH₃OH + H₂O → CO₂ + 6H⁺ + 6e⁻ | کاتالیزگر Pt-Ru (60–80°C) | CO₂، الکترون ها (برق) | تولید توان الکتریکی (پیل سوختی) |
| اکسیداسیون جزئی برای H₂ | CH₃OH + ½ O₂ → CO₂ + 2 H₂ | کاتالیزگر Cu/Zn یا Pt (250°C) | H₂، CO₂ | تولید هیدروژن برای پیل سوختی |
| اکسیداسیون زیستی (آنزیمی) | CH₃OH → CH₂O → HCOOH → CO₂ | آنزیم ها (ADH و غیره)، 37°C | CH₂O، HCOOH، CO₂ | سوخت و ساز در موجودات (مسمومیت متانول) |
| اکسیداسیون فتوکاتالیستی | CH₃OH + O₂ → CO₂ + H₂O | نور UV + کاتالیزگر TiO₂ | CO₂، H₂O | رفع آلودگی محیط (حذف آلاینده ها) |
| اکسیداسیون جوی | CH₃OH + OH• → CH₂O + H₂O | رادیکال های OH (در اثر نور خورشید) | CH₂O، HCOOH، CO₂ | تأثیر بر کیفیت هوا (تشکیل مه دود) |
سازوکار واکنش در اکسیداسیون متانول
در واکنش های مختلف اکسیداسیون متانول، مکانیسم واکنش زیربنایی تفاوت های زیادی دارد. در احتراق، مکانیسم از طریق واکنش های زنجیره ای رادیکالی پیش می رود: حرارت یا جرقه، متانول را به رادیکال های واکنش پذیر (مانند CH₃O• و H• تجزیه می کند که سپس به سرعت با اکسیژن واکنش داده و شعله را گسترش می دهند و در نهایت CO₂ و H₂O تشکیل می شود. در اکسیداسیون کاتالیزی روی سطوح جامد (برای مثال روی نقره یا پلاتین)، مولکول های متانول روی کاتالیزگر جذب سطحی می شوند و به صورت مرحله ای دهیدروژنه می شوند اتم های H جدا شده و حدواسط های جذبی مانند متوکسی (CH₃O) یا فرمالدهید تشکیل می گردد و سپس با اکسیژن روی سطح واکنش داده و محصولات نهایی را ایجاد می کنند. کاتالیزگرها نقش اساسی در کاهش انرژی فعال سازی و جهت دهی مسیر واکنش ایفا می کند (مثلاً ترجیح اکسیداسیون جزئی به فرمالدهید نسبت به احتراق کامل). در اکسیداسیون الکتروشیمیایی (مانند در یک پیل سوختی)، مکانیسم شامل واکنش مولکول های متانول روی سطح الکترود است که طی آن الکترون ها به مدار خارجی کشیده می شوند؛ حدواسط هایی مانند فرمات یا CO روی الکترود جذب می شوند تا زمانی که در مراحل بعد به CO₂ اکسید شوند. اکسیداسیون آنزیمی در موجودات از یک سری مراحل آنزیم محور پیروی می کند: متانول در جایگاه فعال آنزیم قرار گرفته و به فرمالدهید اکسید می شود (در این فرآیند کوآنزیم هایی مانند NAD⁺ الکترون ها را می پذیرند) و سپس در مراحل آنزیمی بعدی به فرمات و CO₂ اکسید می شود. هر مکانیسم در جزئیات متفاوت است اما همگی تحقق تبدیل متانول به گونه های اکسید شده تر را با شکستن پیوندهای C–H و تشکیل پیوندهای O–H یا C–O امکان پذیر می سازند.
کاربردهای صنعتی اکسیداسیون متانول
واکنش های مختلف اکسیداسیون متانول زیربنای کاربردهای صنعتی و تجاری مهمی هستند. بارزترین مثال، تولید فرمالدهید از طریق اکسیداسیون جزئی متانول است که همان طور که پیش تر اشاره شد بخش قابل توجهی از مصرف جهانی متانول را به خود اختصاص می دهد. فرمالدهید حاصل از اکسیداسیون متانول پیش ماده تولید چسب ها، رزین ها و پلاستیک ها است. کاربرد کلیدی دیگر استفاده از متانول به عنوان سوخت است: احتراق متانول (اکسیداسیون آن با هوا) در موتورهای مسابقه ای خاص به کار گرفته می شود و علاقه به استفاده از متانول در حمل و نقل و کشتیرانی به خاطر پاک تر سوختن نسبت به بنزین یا سوخت های سنگین در حال افزایش است. در موتورهای دریایی و دیگ های صنعتی، احتراق متانول می تواند انتشار اکسیدهای گوگرد، اکسیدهای نیتروژن و ذرات معلق را به شدت کاهش دهد. نقش متانول در پیل های سوختی نیز قابل توجه است: چه به صورت مستقیم در سامانه های DMFC و چه به صورت غیرمستقیم با ریفورم کردن به هیدروژن، اکسیداسیون متانول توان الکتریکی تولید می کند. علاوه بر این، تحقیقاتی بر اکسید کردن متانول به سایر مواد شیمیایی مانند دی متیل کربنات یا اسید فرمیک به عنوان روشی برای ذخیره انرژی یا تولید محصولات با ارزش افزوده متمرکز شده است، اگرچه این فرآیندها هنوز در مقیاس وسیع انجام نشده اند. به طور خلاصه، سهولت اکسیداسیون متانول برای تولید گرما، توان و محصولات شیمیایی به کار گرفته می شود و متانول را به ماده ای چند منظوره در صنایع انرژی و شیمیایی تبدیل کرده است.




