فهرست عناوین
- مقدمه
- متانول چیست؟
- ساختار شیمیایی و ترکیب متانول
- حالت فیزیکی و ظاهر متانول
- نقطه جوش و نقطه ذوب متانول
- چگالی و وزن مخصوص متانول
- حلالیت و قابلیت اختلاط متانول
- قطبیت و پیوند هیدروژنی در متانول
- فشار بخار و فراریت متانول
- گرانروی و کشش سطحی متانول
- قابلیت اشتعال و خواص احتراق متانول
- واکنش پذیری و واکنش های شیمیایی متانول
- کاربردهای صنعتی متانول در ارتباط با خواص آن
- خلاصه ای از خواص کلیدی متانول
نوشته شده توسط شرکت صنایع متانول ایران
منتشر شده توسط شرکت صنایع متانول ایران
تاریخ انتشار مقاله : 22-08-1404
تاریخ بروزرسانی مقاله : 22-08-1404
تعداد کلمات : 3200
آدرس مقاله : لینک مقاله
خواص فیزیکی و شیمیایی متانول

مقدمه
متانول که با نام الکل متیلیک یا الکل چوب نیز شناخته می شود، یک الکل ساده با فرمول شیمیایی CH3OH است. این ماده کوچک ترین و ساده ترین عضو خانواده الکل ها است و از یک اتم کربن تشکیل شده که به یک گروه هیدروکسیل (OH) متصل شده است. این مایع شفاف و بی رنگ دارای بوی ملایم الکلی مشابه اتانول است. متانول بسیار قابل اشتعال و سمی است؛ به طوری که حتی مقادیر کم آن در صورت نوشیدن می تواند اثرات جدی بر سلامت داشته باشد. در گذشته متانول از تقطیر خشک چوب به دست می آمد و به همین دلیل نام الکل چوب را به خود گرفته است. امروزه متانول به صورت صنعتی از گاز سنتز (مخلوط مونوکسید کربن و هیدروژن) تولید می شود و به عنوان یک ماده شیمیایی چند منظوره در بسیاری از صنایع به کار می رود. در بسیاری از واحدهای تولیدی، آگاهی از ویژگی ها و کیفیت این ماده نقش مهمی در تصمیم گیری برای خرید متانول دارد، زیرا کاربردهای متنوع آن در سوخت ها، حلال ها و سنتز مواد شیمیایی نیازمند انتخاب محصولی استاندارد و مطمئن است. شناخت خواص فیزیکی و شیمیایی متانول مانند نقطه جوش، حلالیت، واکنش پذیری و سمیت آن برای استفاده ایمن و نیز بهره گیری از کاربردهای فراوان این ماده ضروری است.
متانول چیست؟
در صنایع شیمیایی، متانول بهعنوان یکی از مهم ترین مواد پایه شناخته می شود و نقش کلیدی در تولید بسیاری از ترکیبات آلی دارد. در همین راستا، معرفی متانول و تعاریف اصلی زمانی مفهوم پیدا می کند که ویژگی های ساختاری و عملکردی این ترکیب به صورت دقیق و علمی بررسی شود. متانول یکی از ساده ترین الکل است که در ساختار مولکولی خود تنها یک اتم کربن دارد. از نظر شیمیایی، متانول به عنوان یک الکل نوع اول طبقه بندی می شود و معمولاً به صورت CH3OH یا به اختصار MeOH نشان داده می شود. این ترکیب یک مایع قطبی است که به طور عمومی با نام های دیگری مانند الکل متیلیک، کاربینول یا روح چوب نیز شناخته می شود. متانول به طور طبیعی در مقادیر ناچیز یافت می شود (برای مثال در میوه ها و مایعات تخمیر شده به مقدار کم وجود دارد)، اما به طور معمول در مقیاس صنعتی تولید می شود. به طور سنتی از چوب به دست می آمد، اما تولید مدرن آن از گاز طبیعی یا زغال سنگ از طریق فرآیند گاز سنتز صورت می گیرد. متانول خالص یک مایع شفاف شبیه آب با بویی ملایم و تا حدی شیرین است. به دلیل ساختار ساده و واکنش پذیری بالای خود، متانول به عنوان یک بلوک ساختاری اساسی در شیمی آلی عمل می کند و منجر به تولید موادی مانند فرمالدهید و اسید استیک می شود. همچنین مستقیماً به عنوان سوخت و حلال در کاربردهای گوناگون مورد استفاده قرار می گیرد. با این حال علی رغم شباهت آن از نظر ظاهر و بو به الکل آشامیدنی (اتانول)، متانول برای مصرف خوراکی ایمن نیست و باید با آن همانند یک ماده شیمیایی سمی و اشتعال پذیر رفتار کرد.
ساختار شیمیایی و ترکیب متانول
ساختار شیمیایی متانول از یک گروه متیل (CH3–) متصل به یک گروه هیدروکسیل (–OH) تشکیل شده است. این پیکربندی فرمول مولکولی CH3OH را برای متانول ایجاد می کند که نشان دهنده وجود یک اتم کربن، چهار اتم هیدروژن و یک اتم اکسیژن در هر مولکول است. اتم کربن منفرد در متانول دارای هیبریداسیون sp³ است و با سه اتم هیدروژن خود و گروه هیدروکسیل، ساختار هندسی چهاروجهی تشکیل می دهد. به عنوان ساده ترین الکل آلیفاتیک، متانول پایه ای برای درک الکل های پیچیده تر محسوب می شود. جرم مولکولی آن حدود ۳۲٫۰۴ گرم بر مول است. وجود پیوند قطبی O–H در ترکیب آن به طور قابل توجهی خواص متانول را تحت تاثیر قرار می دهد و به آن قطبیت و توانایی ایجاد پیوند هیدروژنی می بخشد. از نظر ترکیب شیمیایی، متانول یک ترکیب آلی است که صرفاً از کربن، هیدروژن و اکسیژن تشکیل شده و هیچ عنصر دیگری در آن وجود ندارد. این ترکیب ساده بسیاری از ویژگی های آن را توضیح می دهد، از جمله اشتعال پذیری آن (زیرا حاوی عناصر سوختی کربن و هیدروژن است) و اختلاط کامل آن با آب (به دلیل وجود گروه هیدروکسیل قطبی). علاوه بر این اندازه کوچک و داشتن تنها یک گروه هیدروکسیل باعث می شود متانول یک حلال پروتیک قطبی با نیروهای بین مولکولی نسبتاً ضعیف باشد که در نتیجه آن نقطه جوش پایین و فراریت بالایی دارد.
حالت فیزیکی و ظاهر متانول
در شرایط استاندارد (دمای اتاق و فشار معمول)، متانول به صورت مایع است. این یک مایع بی رنگ و شفاف است که از لحاظ ظاهری شبیه آب است. متانول گرانروی نسبتاً کمی دارد و به آسانی جریان می یابد؛ این مایع هیچ باقی مانده روغنی بر جای نمی گذارد و به همین دلیل گاهی افراد آن را با آب یا اتانول اشتباه می گیرند. این مایع بوی الکلی دارد که ملایم و اندکی شیرین است و مشابه بوی اتانول (الکل نوشیدنی) می باشد. متانول خالص هیچ رنگ یا کدورتی ندارد و کاملاً زلال به نظر می رسد. در واقع، ضریب شکست نوری آن تقریباً با آب یکسان است و باعث می شود تشخیص ظاهری متانول در ظروف شیشه ای از آب دشوار باشد. از آنجا که متانول بسیار فرار است، حتی در دمای اتاق نیز به راحتی بخار تولید می کند اما این بخارات نیز بی رنگ هستند و به آسانی دیده نمی شوند. یکی از جنبه های قابل توجه ظاهر متانول این است که هنگام سوختن، شعله ای آبی کم رنگ تولید می کند که در روشنایی روز تقریباً نامرئی است. اگرچه متانول بی خطر به نظر می رسد، اما ظاهر آن فریبنده است زیرا این ماده قابل اشتعال و سمی می باشد. این واقعیت که شبیه آب یا الکل معمولی به نظر می رسد به این معناست که در کار کردن با آن باید احتیاط کرد تا از بلع یا تماس تصادفی جلوگیری شود.
نقطه جوش و نقطه ذوب متانول
متانول دارای نقطه جوش پایینی در حدود ۶۴٫۷ درجه سانتیگراد در فشار جو است. این بدان معناست که متانول در دمای بسیار پایین تری نسبت به آب (که در ۱۰۰ درجه سانتیگراد به جوش می آید) از مایع به گاز تبدیل می شود و نشان دهنده فراریت بالای متانول است. در نتیجه، متانول حتی با گرم شدن ملایم یا در یک روز گرم نیز به راحتی به جوش می آید یا تبخیر می شود و به سرعت بخار تولید می کند. نقطه جوش پایین آن به دلیل وزن مولکولی کم و داشتن فقط یک گروه هیدروکسیل می باشد که باعث پیوند هیدروژنی کمتری بین مولکول های متانول در مقایسه با آب یا الکل های بزرگ تر می شود. در سوی دیگر طیف، نقطه انجماد (ذوب) متانول حدود منفی ۹۷٫۶ درجه سانتیگراد است. این نقطه ذوب فوق العاده پایین نشان می دهد که متانول در شرایط بسیار سرد به صورت مایع باقی می ماند؛ این ماده تا زمانی که دماها بسیار پایین تر از زمستان های معمول شوند یخ نمی زند. چنین نقطه انجماد پایینی یکی از دلایلی است که متانول در کاربردهای ضدیخ مورد استفاده قرار می گیرد. دامنه دمایی وسیع حالت مایع متانول (از منفی ۹۷٫۶ تا ۶۴٫۷ درجه سانتیگراد در فشار ۱ اتمسفر) نشان دهنده توانایی متانول در مایع ماندن در بازه گسترده ای از دماهای متداول است و این امر کار کردن با آن را به عنوان یک سوخت و حلال مایع آسان می سازد.
چگالی و وزن مخصوص متانول
چگالی متانول کمتر از آب است. در دمای حدود ۲۰ درجه سانتیگراد، چگالی آن تقریباً ۰٫۷۹ گرم بر سانتی متر مکعب (یا ۷۹۰ کیلوگرم بر متر مکعب) است، در حالی که چگالی آب در همین دما ۱٫۰۰ گرم بر سانتی متر مکعب می باشد. این بدان معنی است که وزن مخصوص متانول (نسبت چگالی آن به چگالی آب) حدود ۰٫۷۹ است. به عبارتی دیگر، یک حجم معین از متانول تقریباً ۲۱٪ سبک تر از همان حجم آب است. چگالی کم متانول نتیجه ساختار مولکولی سبک تر و نیروهای بین مولکولی ضعیف تر آن است (در مقایسه با آب که شبکه های گسترده ای از پیوندهای هیدروژنی تشکیل می دهد). از آنجا که متانول کاملاً با آب قابل اختلاط است، معمولاً هنگام مخلوط شدن لایه های جداگانه ای تشکیل نمی دهد؛ اما اگر چنین بود، به دلیل سبک تر بودن روی لایه آبی شناور می ماند. دانستن چگالی متانول برای کاربردهای مختلف مهم است به عنوان مثال، در اختلاط سوخت ها و واکنش های شیمیایی که در آنها تبدیل حجم به جرم مورد نیاز است. وزن مخصوص نسبتاً کم متانول همچنین بر نحوه رفتار آن در جریان و حمل و نقل تأثیر می گذارد، زیرا در مقایسه با آب یا مایعات آلی سنگین تر، وزن کمتری در هر گالن یا لیتر اعمال می کند.
حلالیت و قابلیت اختلاط متانول
متانول در آب بسیار محلول است در واقع کاملاً قابل امتزاج بوده و می تواند در هر نسبتی بدون جدا شدن با آب مخلوط شود. وقتی متانول به آب اضافه می شود، این دو مایع به طور یکنواخت با هم مخلوط می شوند و یک فاز مایع یکدست ایجاد می شود. این امتزاج پذیری کامل به دلیل قطبیت متانول و توانایی آن در ایجاد پیوند هیدروژنی با مولکول های آب است. گروه هیدروکسیل (–OH) در متانول با مولکول های H2O آب پیوند هیدروژنی تشکیل می دهد و به دو ماده اجازه می دهد در سطح مولکولی با هم ادغام شوند. متانول نه تنها با آب امتزاج پذیر است، بلکه با بسیاری از حلال های آلی دیگر نیز به خوبی مخلوط می شود. این ماده با اتانول، اتر دی اتیل، استون، کلروفرم و اغلب الکل ها و حلال های قطبی دیگر قابل امتزاج است. حتی در برخی حلال های غیرقطبی، متانول به دلیل اندازه کوچک خود حلالیت متوسطی دارد، اگرچه در موادی مانند روغن ها یا هگزان به میزان قابل توجهی حل نمی شود. علاوه بر این، متانول می تواند طیف گسترده ای از ترکیبات آلی و برخی نمک های معدنی را حل کند و به همین دلیل یک حلال مفید در آزمایشگاه و صنعت است. قابلیت حلالیت گسترده آن یکی از دلایلی است که متانول به طور گسترده ای به عنوان حلال و جزو ترکیبات ضدیخ مورد استفاده قرار می گیرد.
قطبیت و پیوند هیدروژنی در متانول
متانول یک مولکول قطبی است زیرا وجود اتم اکسیژن الکترونگاتیو و پیوند O–H در آن چنین خاصیتی را ایجاد می کند. اکسیژن چگالی الکترون را به سمت خود می کشد و بار منفی جزئی بر روی اتم اکسیژن و بار مثبت جزئی بر روی اتم هیدروژن گروه هیدروکسیل ایجاد می کند. این قطبیت به این معناست که مولکول های متانول به یکدیگر و به سایر مولکول های قطبی (از جمله آب) جذب می شوند. یکی از پیامدهای مهم این قطبیت، توانایی متانول در تشکیل پیوند هیدروژنی است. متانول می تواند یک پیوند هیدروژنی را اهدا کند از طریق اتم هیدروژن گروه–OH خود و پیوندهای هیدروژنی را بپذیرد (از طریق جفت الکترون های ناپیوندی روی اتم اکسیژن خود). در متانول مایع هر مولکول ممکن است با مولکول های مجاور پیوند هیدروژنی تشکیل دهد، اگرچه هر مولکول متانول نسبت به یک مولکول آب پیوندهای هیدروژنی کمتری می تواند تشکیل دهد. این پیوندهای هیدروژنی بین مولکولی باعث می شوند نقطه جوش متانول بالاتر از حالتی باشد که کاملاً غیرقطبی می بود. با این حال هر مولکول متانول تنها قادر به اهدا کردن یک پیوند هیدروژنی است (در حالی که هر مولکول آب قادر به اهدا کردن دو پیوند است) و این محدودیت در شبکه پیوند هیدروژنی آن باعث می شود متانول نسبت به آب فرارتر باشد. قطبیت قوی و توانایی پیوند هیدروژنی متانول، قدرت حلالیت عالی آن برای بسیاری از مواد قطبی و قابلیت امتزاج کامل آن با آب را توضیح می دهد.
فشار بخار و فراریت متانول
متانول در دماهای محیطی دارای فشار بخار بالایی است که معیاری برای سنجش تمایل آن به تبخیر شدن است. در ۲۰ درجه سانتیگراد، فشار بخار متانول حدود ۱۳ کیلوپاسکال است که بسیار بالاتر از فشار بخار آب (حدود ۲٫۳ کیلوپاسکال در ۲۰ درجه سانتیگراد) می باشد. این نشان می دهد که متانول به راحتی تبخیر می شود و می تواند در ظروف باز غلظت بخار قابل توجهی ایجاد کند. متانول حتی در دمای اتاق سریع تبخیر می کند و بخار آن در صورت تهویه نامناسب می تواند یک فضای بسته را پر کند. فراریت بالای متانول مستقیماً با نقطه جوش پایین و نیروهای بین مولکولی نسبتاً ضعیف آن مرتبط است. از آنجا که بخار متانول قابل اشتعال و سنگین تر از هوا است، ممکن است در نزدیکی سطح زمین نشست کرده و تجمع یابد و در صورت وجود منبع جرقه، خطر آتش سوزی ایجاد کند. بوی الکلی قوی متانول اغلب هنگام تبخیر آن قابل استشمام است و به عنوان هشداری برای حضور آن در هوا عمل می کند. کار کردن با متانول نیاز به احتیاط دارد تا از استنشاق بخارات غلیظ و تجمع بخار در اطراف منابع جرقه جلوگیری شود. فراریت بالا همچنین به این معنی است که متانول باید در ظروف کاملاً سربسته ذخیره شود تا اتلاف آن به حداقل برسد و خطر حریق کاهش یابد.
گرانروی و کشش سطحی متانول
متانول مایعی بسیار روان با گرانروی کم است. در دمای ۲۰ درجه سانتیگراد، گرانروی آن حدود ۰٫۶ سانتی پوآز است (حدود نیمی از گرانروی آب در همین دما). این به آن معناست که متانول به آسانی جریان می یابد و می تواند نسبت به مایعات گرانروتر راحت تر به منافذ و شکاف های ریز نفوذ کند. گرانروی پایین آن به دلیل اندازه کوچک مولکول هایش و پیوند هیدروژنی محدود بین آنها است که مقاومت کمی در برابر جریان ایجاد می کند. علاوه بر گرانروی پایین، متانول دارای کشش سطحی نسبتاً پایینی نیز می باشد. کشش سطحی متانول در دمای اتاق حدود ۲۲ تا ۲۳ میلی نیوتن بر متر است که تقریباً یک سوم کشش سطحی آب (که حدود ۷۲ میلی نیوتن بر متر است) می باشد. این کشش سطحی پایین به این معنی است که متانول روی سطوح پخش می شود و مواد را مؤثرتر از آب تر می کند، به جای اینکه به صورت قطره قطره جمع شود. در نتیجه متانول می تواند یک فیلم نازک و پیوسته روی سطوح تشکیل دهد. ترکیب گرانروی کم و کشش سطحی پایین به اثربخشی متانول به عنوان یک عامل پاک کننده و حلال کمک می کند، زیرا می تواند سطوح را پوشش دهد و به درزها نفوذ کند و تماس خوبی با موادی که قرار است تمیز یا حل شوند برقرار نماید.
قابلیت اشتعال و خواص احتراق متانول
متانول به شدت قابل اشتعال است و به راحتی در هوا می سوزد. نقطه اشتعال آن حدود ۱۱ درجه سانتیگراد (حدود ۵۲ درجه فارنهایت) است، به این معنی که در دماهای کمی بالاتر از دمای اتاق می تواند به اندازه کافی بخار تولید کند تا مشتعل شود. آتش متانول با شعله آبی کم رنگی می سوزد که ممکن است در روشنایی روز دیدنش دشوار باشد. هنگامی که به طور کامل می سوزد، متانول با اکسیژن واکنش می دهد و دی اکسید کربن و آب تشکیل می دهد ۲ CH3OH + 3 O2 → 2 CO2 + 4 H2O و انرژی حرارتی آزاد می کند. اما احتراق ناقص می تواند منجر به تولید مونوکسید کربن و فرمالدهید شود. یک نکته مهم ایمنی این است که شعله متانول همیشه قابل مشاهده نیست و اگر دقت نشود می تواند منجر به سوختگی تصادفی گردد. بخارهای آن نیز می توانند مشتعل شوند و دامنه اشتعال آن در هوا نسبتاً گسترده است (حدود ۶٪ تا ۳۶٪ متانول در هوا). متانول قابل اشتعال است و باید با احتیاط جابجا می شود، به ویژه در نزدیکی شعله های باز یا سطوح داغ. یکی از مزایا در شرایط آتش سوزی این است که متانول با آب قابل اختلاط است، بنابراین می توان از آب برای رقیق کردن و خاموش کردن آتش متانول به طور مؤثر استفاده کرد. با این حال به دلیل سهولت اشتعال این مایع، باید تدابیر ایمنی مناسب در برابر آتش اتخاذ شود.
واکنش پذیری و واکنش های شیمیایی متانول
متانول به دلیل داشتن گروه عاملی الکل و ساختار ساده خود چندین واکنش شیمیایی مهم از خود نشان می دهد. یکی از واکنش های عمده، اکسیداسیون است: متانول می تواند با استفاده از کاتالیزورها یا آنزیم های مناسب به فرمالدهید (CH2O) و در ادامه به اسید فرمیک (HCOOH) اکسید شود. اگر به طور کامل اکسید شود (مانند در احتراق)، متانول با اکسیژن واکنش می دهد و دی اکسید کربن و آب به همراه گرما تولید می کند. در حضور اسیدهای قوی (مانند اسید سولفوریک غلیظ)، متانول می تواند آبگیری شده و دی متیل اتر (CH3OCH3) تولید کند. همچنین با اسیدهای آلی یا انیدریدهای اسیدی واکنش می دهد و استرهای متیل تشکیل می دهد به عنوان مثال، واکنش متانول با اسید استیک، متیل استات تولید می کند. پیوند O–H در متانول می تواند به عنوان یک اسید بسیار ضعیف عمل کند؛ برای مثال، متانول با فلزات فعالی مانند سدیم یا پتاسیم واکنش داده، گاز هیدروژن آزاد می کند و متوکسید فلز (مانند متوکسید سدیم) تشکیل می دهد. متانول حتی می تواند در واکنش های ترانس استریفیکاسیون (تبادل گروه های الکلی در استرها) شرکت کند، فرآیندی که به طور صنعتی برای تولید بیودیزل از روغن های چرب به کار می رود. در مجموع متانول با وجود اینکه یک مولکول کوچک نسبتاً پایدار است، اما می تواند تحت شرایط و کاتالیزورهای مناسب به بسیاری از مواد شیمیایی دیگر تبدیل شود.
کاربردهای صنعتی متانول در ارتباط با خواص آن
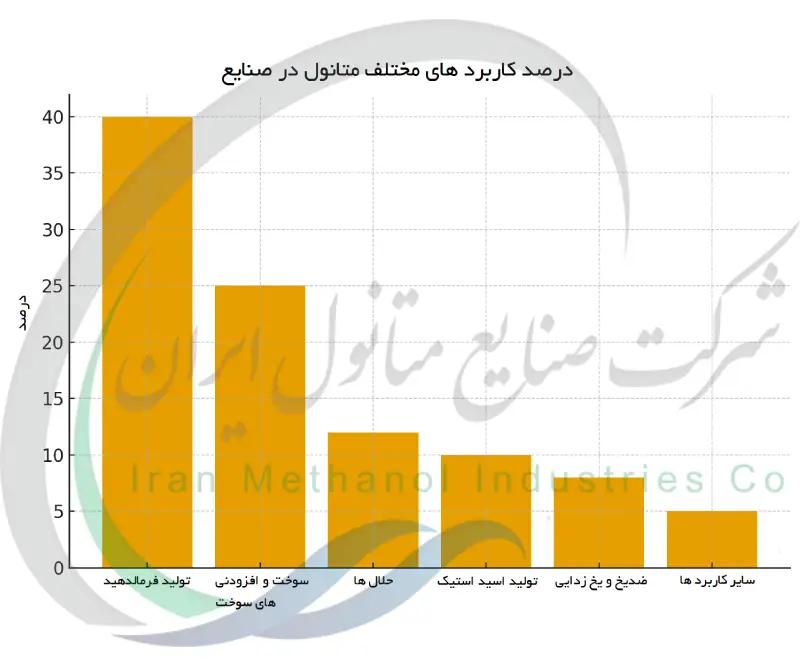
خواص فیزیکی و شیمیایی متانول آن را به ماده ای ارزشمند در بسیاری از صنایع تبدیل کرده است. یکی از کاربردهای مهم آن به عنوان ماده خام شیمیایی است: متانول به فرمالدهید، اسید استیک، متیل ترت بوتیل اتر (MTBE) و سایر مواد شیمیایی صنعتی مهم تبدیل می شود. قابلیت اشتعال و سوختن پاک آن موجب شده است که متانول به عنوان سوخت یا افزودنی سوخت مورد استفاده قرار گیرد. متانول به بنزین افزوده می شود تا عدد اکتان را بالا ببرد (برخی سوخت ها حاوی حدود ۱۰٪ تا ۱۵٪ متانول هستند) و در موتورهای مسابقه ای با کارایی بالا برای احتراق خنک تر به کار رفته است. به دلیل نقطه انجماد پایین، متانول به عنوان ماده ضدیخ در مایع شیشه شور خودروها و در خطوط لوله گاز طبیعی (برای جلوگیری از تشکیل یخ) عمل می کند. خواص حلالیت عالی متانول (قطبی بودن و قابل امتزاج بودن با آب و بسیاری از مواد آلی) باعث شده است از آن به عنوان حلال برای رنگ ها، رزین ها، جوهرها و چسب ها استفاده شود. همچنین در آزمایشگاه ها برای استخراج ترکیبات و به عنوان ماده دناتوره کننده اتانول (برای غیر قابل شرب کردن آن) استفاده می شود. در تصفیه فاضلاب، گاهی متانول به عنوان منبع کربن اضافه می شود تا به باکتری ها در حذف نیترات ها از طریق فرایند نیترات زدایی کمک کند. گستردگی کاربردهای متانول مستقیماً به خواص آن مربوط است فراریت، قابلیت حلالیت، اشتعال پذیری و واکنش پذیری آن امکان به کارگیری آن را در گستره ای از زمینه ها از انرژی گرفته تا تولید مواد شیمیایی فراهم می کند.
خلاصه ای از خواص کلیدی متانول
متانول یک مایع سبک، فرار و قابل اشتعال است که ساده ترین نمونه از یک الکل به شمار می رود. از ویژگی های آن می توان به نقطه جوش پایین (حدود ۶۴٫۷ درجه سانتیگراد) و نقطه انجماد بسیار پایین (حدود ۹۷٫۶- درجه سانتیگراد) اشاره کرد که نشان می دهد متانول در گستره وسیعی از دما مایع باقی می ماند. این مایع از آب سبک تر است (چگالی نسبی ~۰٫۷۹) و به طور کامل با آب قابل اختلاط است. از نظر شیمیایی، ساختار تک کربنه و گروه هیدروکسیل متانول به آن قطبیت می بخشند و امکان ایجاد پیوند هیدروژنی و قابلیت حلالیت را فراهم می کنند، همچنین این ویژگی ها متانول را قابل احتراق و از نظر شیمیایی واکنش پذیر (تحت شرایط مناسب) می سازند. جدول زیر برخی از مهم ترین خواص فیزیکی و شیمیایی متانول را برای مرور سریع خلاصه می کند:
| مشخصه | مقدار | واحد | شرایط | توضیحات |
|---|---|---|---|---|
| فرمول شیمیایی | CH₃OH | – | – | ساده ترین الکل (یک اتم کربن) |
| جرم مولکولی | ۳۲٫۰۴ | گرم/مول | – | جرم یک مول مولکول های CH₃OH |
| نقطه جوش | ۶۴٫۷ | °C | در ۱ اتمسفر | نقطه جوش پایین، مایع بسیار فرار |
| نقطه ذوب | ۹۷٫۶- | °C | در ۱ اتمسفر | در دمای بسیار پایین منجمد می شود |
| چگالی | ۰٫۷۹۲ | گرم/سانتی متر³ | در ۲۰°C | سبک تر از آب (چگالی نسبی ~۰٫۷۹) |
| حلالیت در آب | قابل اختلاط | – | ۲۰°C (دمای اتاق) | در تمام نسبت ها با آب مخلوط می شود |
| نقطه اشتعال | ~۱۱ | °C | در تست بسته | به آسانی در دمای پایین مشتعل می شود |





بررسی خواص فيزيكي متانول شامل فراريت بالا ، چگالي كم ، نقطه اشتعال پايين و انحلال پذيري كامل در آب
بررسی خواص شیمیایی متانول و کاربرد آن به عنوان سوخت
بررسی قابلیت اشتعال و انرژی زایی متانول و ملاحظات ایمنی در برابر آتش سوزی این ماده
بررسی خواص سمی و بیولوژیکی متانول و کاربردهای رایج آن